
下列离子方程式书写不正确的是( )
A.NaOH溶液与SO2反应,当n(NaOH):n(SO2)=4:3时:4OH- + 3SO2 = SO32-+ 2HSO3- + H2O
B.CuCl2溶液与Na2S溶液2:1反应,Cu2++ S2-= CuS↓
C.Cl2与FeBr2溶液反应,当n(Cl2):n(FeBr2)=1:1时:2Fe2+ + 4Br- +3Cl2 = 2 Fe3+ + 2Br2 + 6Cl-
D.1mol/L的NaAlO2溶液和2.5mol/L的HCl等体积互相均匀混合:2AlO2-+5H+=Al(OH)3↓+Al3++H2O
科目:高中化学 来源:2016-2017学年福建省高一上学期第一次月考化学试卷(解析版) 题型:选择题
下列关于研究物质性质的基本程序,排列顺序正确的是
a.观察物质的外观性质 b.实验和观察 c.解释及结论 d.预测物质的性质
A.bacd B.abcd C.adbc D.dabc
查看答案和解析>>
科目:高中化学 来源:2017届江苏省高三上期初考试化学试卷(解析版) 题型:选择题
在探究SO2水溶液成分和性质的实验中,下列根据实验现象得出的结论正确的是
A. 向SO2水溶液中加入少量NaHCO3粉末,有气泡产生,说明SO2水溶液呈酸性
B. 向SO2水溶液中滴加Ba(NO3)2溶液,有白色沉淀产生,说明SO2水溶液中含有SO42-
C. 将SO2水溶液中通入H2S气体,有淡黄色沉淀产生,说明SO2水溶液具有氧化性
D. 向KMnO4溶液中滴加SO2水溶液,溶液颜色褪去,说明SO2水溶液具有漂白性
查看答案和解析>>
科目:高中化学 来源:2017届河北省高三小二调考化学试卷(解析版) 题型:实验题
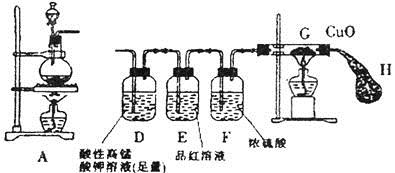
实验目的:研究铁与浓硫酸的反应
实验药品:铁钉、浓硫酸、酸性KMnO4溶液,品红溶液、CuO
实验步骤:
实验步骤 | 实验现象 | 结论 |
将铁钉(足量)加入烧瓶中,再向其中滴加含amol硫酸的浓硫酸溶液 | 未见明显现象 | 原因: |
点燃A、G处酒精灯 | 片刻后,烧瓶中溶液的颜色发生变化,并有气泡产生。 | 烧瓶中发生的所有反应 |
填完上述实验报告并回答下列问题:
(1)连接好装置后,盛放药品前,首先要进行 操作。
(2)为了测定产生的SO2的量,实验后向烧瓶中加足量的盐酸至无气泡产生,再加足量的BaCl2溶液至沉淀完全,为判断沉淀完全,应该进行的操作是: ,然后进行过滤、洗涤、干燥、称量。
(3)若(2)中所得沉淀的质量为mg,则反应产生的SO2在标准状况的体积为(列出计算式即可): L
查看答案和解析>>
科目:高中化学 来源:2017届河北省高三小二调考化学试卷(解析版) 题型:选择题
海带中的碘元素是以I-的形式存在的,为将I-转化成I2并提取出来,设计操作步骤如下:①通入Cl2;②将海带烧成灰,向灰中加水,搅拌;③加CCl4振荡;④过滤;⑤用分液漏斗分液。合理的操作顺序为( )
A. ①③⑤②④ B. ②①③④⑤ C. ②④①③⑤ D. ③①②⑤④
查看答案和解析>>
科目:高中化学 来源:2017届河北省高三小二调考化学试卷(解析版) 题型:选择题
工业上用固体硫酸亚铁制取颜料铁红,反应原理是:2FeSO4  Fe2O3+SO2↑+SO3↑。某学生欲检验该反应所产生的气态物质,他依次将气体通过盛有(I)BaCl2溶液、( II ) x 溶液、(III)NaOH 溶液的三个装置。则下列对该方案的评价中正确的是 ( )
Fe2O3+SO2↑+SO3↑。某学生欲检验该反应所产生的气态物质,他依次将气体通过盛有(I)BaCl2溶液、( II ) x 溶液、(III)NaOH 溶液的三个装置。则下列对该方案的评价中正确的是 ( )
A.(I)中会生成 BaSO3、BaSO4两种沉淀
B.可将(I)中的 BaCl2溶液改为 Ba ( NO3 )2溶液
C.(II)所盛 x应为品红溶液
D.( III)的作用是检验生成的SO2 气体
查看答案和解析>>
科目:高中化学 来源:2017届河北省高三小二调考化学试卷(解析版) 题型:选择题
某溶液既能溶解Al(OH)3,又能溶解H2SiO3,在该溶液中可以大量共存的离子组是( )
A.Na+、SO42-、 、ClO- B.K+、Na+、HCO3-、NO3-
、ClO- B.K+、Na+、HCO3-、NO3-
C.H+、Mg2+、SO42-、NO3- D.Ag+、K+、NO3-、Na+
查看答案和解析>>
科目:高中化学 来源:2017届河北省等五校高三上学期第一次模拟化学试卷(解析版) 题型:选择题
一定温度下,在甲、乙、丙、丁四个恒容密闭容器中投入SO2(g)和O2(g),进行反应,
2SO2+O2 2SO3,其起始物质的量及SO2的平衡转化率如下表所示。下列判断中正确的是
2SO3,其起始物质的量及SO2的平衡转化率如下表所示。下列判断中正确的是
甲 | 乙 | 丙 | 丁 | ||
密闭容器体积/L | 2 | 2 | 2 | 1 | |
起始物质的量 | n(SO2)/mol | 0.40 | 0.80 | 0.80 | 0.40 |
n(O2)/mol | 0.24 | 0.24 | 0.48 | 0.24 | |
SO2的平衡转化率% | 80 |
|
|
| |
A.甲中反应的平衡常数小于乙
B.该温度下,该反应的平衡常数K为400
C.SO2的平衡转化率: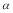 1>
1>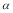 2 =
2 = 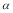 3
3
D.容器中SO3的物质的量浓度:丙=丁<甲
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高二上学期第一次月考化学试卷(解析版) 题型:选择题
一定温度下,反应N2(g)+O2(g)===2NO(g)在密闭容器中进行,下列措施不改变化学反应速率的是( )
A.缩小体积使压强增大 B.恒容,充入N2
C.恒容,充入He D.恒压,充入He
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com