
氧化铝中含少量氧化铁和二氧化硅杂质,试写出除杂过程和有关的化学方程式。
(1)将样品加稍过量的盐酸中充分反应,过滤除去SiO2:Al2O3+6HCl=2AlCl3+3H2O;Fe2O3+6HCl=2FeCl3+3H2O。
(2)向滤液中加稍过量的氢氧化钠溶液,充分反应后过滤,除去Fe(OH)3。
NaOH+HCl=NaCl+H2O;3NaOH+FeCl3=Fe(OH)3↓+3NaCl;4NaOH+AlCl3=Na[Al(OH)4]+3NaCl
(3)向上述滤液中通入过量二氧化碳,过滤,得Al(OH)3
CO2+NaOH=NaHCO3;Na[Al(OH)4]+CO2=Al(OH)3↓+NaHCO3。
(4)将所得Al(OH)3加热得Al2O3。2 Al(OH)3![]() Al2O3+3H2O
Al2O3+3H2O
本题的特点是:两性氧化物中含有碱性氧化物和酸性氧化物的杂质。应根据三类不同氧化物与酸、碱反应的情况加以分析。氧化铝与强酸、强碱都反应,除杂时必然转化为其它物质。应选择适当的酸、碱将杂质一一除去,并使氧化铝复生。


科目:高中化学 来源: 题型:阅读理解

| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Al(OH)3 |
| 开始沉淀 | 2.3 | 7.5 | 3.4 |
| 完全沉淀 | 3.2 | 9.7 | 4.4 |
 [Fe2(OH)4]2++2H+
[Fe2(OH)4]2++2H+ [Fe2(OH)4]2++2H+
[Fe2(OH)4]2++2H+
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
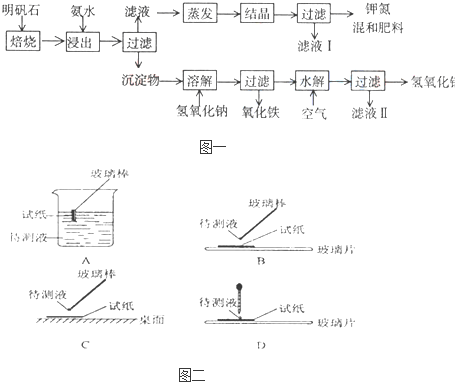
| (m-132n) |
| 42 |
| (m-132n) |
| 42 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
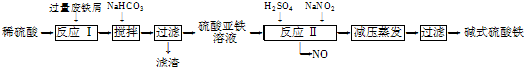
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Al(OH)3 |
| 开始沉淀 | 2.3 | 7.5 | 3.4 |
| 完全沉淀 | 3.2 | 9.7 | 4.4 |
2+ 4 |
- 3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com