
_____________________________________________________________________
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
溶氧分析仪能连续、自动测量水中微量的溶解氧含量,可用于工业锅炉用水,实验室制备除氧水等方面。溶氧分析仪的核心部件是氧传感器,传感器中银做阳极,金做阴极,二电极之间连接一稳定的直流电源,以氯化钾溶液为电解质溶液,电解质溶液与取样水之间有一层氧气可以透过的薄膜,测量金电极上产生的还原电流的大小得出氧气的含量。
⑴ 试写出溶氧分析仪的有关电极反应式
阴极_______________________________,阳极____________________________________
⑵ 请从你写的电极反应式推测影响氧传感器的性能的因素可能有哪些?
在高温下高炉中氧含量的测定可用氧化锆(ZrO2)氧传感器来测定,在氧化锆中加入MgO,Y2O3等立方晶系的氧化物后,在600℃以上高温时成为氧的快离子导体。其导电性能主要源于掺杂晶体中的氧离子空位。下图为氧化锆固体电解质的导电原理。
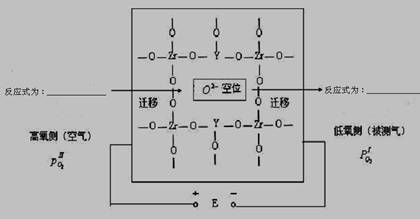
⑶ 写出高氧侧和低氧侧的电极反应式
高氧侧______________________________,低氧侧________________________________
⑷ 若某掺杂电极Y2O3的ZrO2晶体中氧离子空位数为3.01×1020个,则理论上掺杂的Y2O3质量为多少克?
查看答案和解析>>
科目:高中化学 来源:2014届陕西省高一上学期期末试题化学(理)试卷 题型:填空题
(15分)铁及其化合物在国民经济、日常生活中占有非常重要的地位,了解铁及其化合物的性质和用途非常重要。请回答下列问题:
(1)铁在自然界中以 态存在,其氧化物呈黑色的是 ,呈红褐色的是 (填写化学式)。
(2)铁在纯氧气中燃烧的化学方程式为 。
铁在氯气中反应的产物是 。
(3)要验证一种溶液中是否含有Fe3+、Fe2+,正确的实验方法是 。
A.向甲试管中加入试液,滴入KSCN溶液,若显血红色,证明一定存在Fe3+。
B.向乙试管中加入试液,滴入氯水,若氯水褪色,证明一定存在Fe2+。
C.向丙试管中加入试液,滴入氯水,再滴入KSCN溶液,若显血红色,证明原溶液中一定存在Fe3+
(4)铁合金有下列数据:
|
钢 |
|||
|
碳素钢(Fe、C、Mn、Si) |
合金钢 |
||
|
低碳钢 |
中碳钢 |
高碳钢 |
碳素钢+Cr、Mn、W、Ni、Co等 |
|
含碳量<0.3% |
含碳量0.3%--0.6% |
含碳量>0.6% |
|
|
韧性好,强度低 |
韧性好、强度好 |
硬而脆 |
具有特殊性能 |
取15g某碳素钢样品,按下列实验流程进行操作:

①A、B的作用是 ,
②充分加热完全反应后,D装置质量增加0.022g,该样品属于 钢。
③没有A、B装置,实验结果 (填“偏高”“偏低”“不影响”)
查看答案和解析>>
科目:高中化学 来源: 题型:
______________________________________________________________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com