
���� ��1��1.0 mol/L Fe2��SO4��3��Һ��Fe3+�����ʵ���Ũ��Ϊ2mol/L��SO42-��Ũ��Ϊ3mol/L��2.0mol/L CuSO4��Һ��SO42-��Ũ��Ϊ2mol/L������ϡ�Ͷ��ɼ��㣻
��2�����������ԣ�Fe3+��Cu2+�������Fe����Fe3+��Ӧ����Ӧ����Һ�е�Fe2+���ʵ���Ũ�ȵ���Fe3+�����ʵ���Ũ�ȣ���Cu2+δ�μӷ�Ӧ�����Fe+2 Fe3+=3 Fe2+���㣮
��� �⣺��1��1.0 mol/L Fe2��SO4��3��Һ��Fe3+�����ʵ���Ũ��Ϊ2mol/L��SO42-��Ũ��Ϊ3mol/L��2.0mol/L CuSO4��Һ��SO42-��Ũ��Ϊ2mol/L���������Ϻ���Һ�е�Fe3+�����ʵ���Ũ��Ϊ2mol/L��$\frac{1}{2}$=1mol/L������Һ�������Ϊ1L����Ϻ���Һ��SO42-�����ʵ���Ũ��Ϊ$\frac{1L��2mol/L+1L��3mol/L}{2L}$=2.5 mol/L��
�ʴ�Ϊ��1mol/L��2.5mol/L��
��2�����������ԣ�Fe3+��Cu2+�������Fe����Fe3+��Ӧ����Ӧ����Һ�е�Fe2+���ʵ���Ũ�ȵ���Fe3+�����ʵ���Ũ�ȣ���Cu2+δ�μӷ�Ӧ��500mL�����Һ��Fe3+�����ʵ���Ϊ0.5L��1mol/L=0.5mol��
������FeΪx mol����
Fe+2 Fe3+=3 Fe2+
x mol 2x mol 3x mol
���ԣ�3x=0.5-2x
���x=0.1
�ʼ���Fe������Ϊ0.1mol��56g/mol=5.6g��
�ʴ�Ϊ��5.6��
���� ���⿼�����ʵ���Ũ�ȵ��йؼ��㡢��ѧ����ʽ�ļ���ȣ�ע������ʵ����Ѷȹ�ʽ��������������ã���2���йؼ����жϷ�Ӧ�Ⱥ�˳�����⣮


 �Ͻ�ƽСѧ��������ϵ�д�
�Ͻ�ƽСѧ��������ϵ�д� �Ƹ������������ϵ�д�
�Ƹ������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���߶�Ӧ���������Ϊ���������� | |
| B�� | ���ߵĵ��ʶ�����������������Һ��Ӧ | |
| C�� | ���������£����ֽ��������ܽ���Ũ������ | |
| D�� | �Ʊ�AlCl3��FeCl3�������ܲ��ý�����Һֱ�����ɵķ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ${\;}_{92}^{235}$Uԭ�Ӻ��к���92������ | B�� | ${\;}_{92}^{235}$Uԭ�Ӻ�����143������ | ||
| C�� | ${\;}_{92}^{235}$U��������Ϊ92 | D�� | ${\;}_{92}^{235}$U��${\;}_{92}^{238}$U��Ϊͬλ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
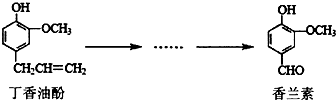 ����������Ҫ������֮һ�������ɶ����ͷӾ��ಽ��Ӧ�ϳɣ�����ͼ�����й��������ֻ������˵������ȷ���ǣ�������
����������Ҫ������֮һ�������ɶ����ͷӾ��ಽ��Ӧ�ϳɣ�����ͼ�����й��������ֻ������˵������ȷ���ǣ�������| A�� | �ڶ����ͷӷ�����������12��ԭ�ӹ�ƽ�� | |
| B�� | �����£�1mol�����ͷӿ���2molBr2��Ӧ | |
| C�� | 1moI�������������4mol���������ӳɷ�Ӧ | |
| D�� | ��������KMnO4��Һ���鶡���ͷ����Ƿ���̼̼˫�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | RO | B�� | R2H4 | C�� | HRO2 | D�� | H2R2O4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
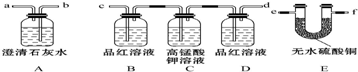
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 2-�������2-��-1-��ϩ | B�� | CH3��CH2��2CH3��CH3C��CH3��2CH3 | ||
| C�� | 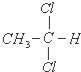 �� �� | D�� |  �� ��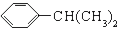 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���³�ѹ�£�40gSiC�к���Si-C������ĿΪNA | |
| B�� | ��״���£�5.6LO2����4 NA������ | |
| C�� | 53.5gNH4Cl�к���H-Cl������ĿΪ4NA | |
| D�� | 25��ʱ��pH=13��1L Ba��OH��2��Һ�к���OH-����ĿΪ0.2NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ����� | ǿ����� | ������� | �ǵ���� | |
| A | ��ˮ | H2SO4 | CH3COOH | �ɱ� |
| B | ���� | �������� | H2SO4 | SO2 |
| C | ���� | BaSO4 | H2S | ���� |
| D | ����������Һ | ʯ��ʯ | ����NaCl | ���� |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com