
| A. | 常温下能溶于水 | B. | 水溶液能导电 | C. | 熔融状态能导电 | D. | 具有较高的熔点 |
分析 离子化合物中一定含有离子键,要证明氯化钠中一定含有离子键,只要证明熔融态氯化钠能导电即可,以此解答该题.
解答 解:A.能溶于水的物质不一定含有离子键,如氨气、HCl等,故A错误;
B.水溶液能导电的物质不一定含有离子键,如硫酸、硝酸等,故B错误;
C.离子化合物在熔融态能电离出自由移动的阴阳离子而导电,共价化合物熔融态以分子存在而不导电,故C正确;
D.熔沸点较高的物质不一定含有离子键,如钨丝、金刚石等,故D错误;故选C.
点评 本题考查离子键的判断,为高频考点,侧重考查学生的分析能力,可以根据离子化合物和共价化合物熔融态是否导电判断,注意不能根据溶解性强弱、水溶液导电能力强弱判断,为易错点.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 同一周期元素的原子,半径越小越容易失去电子 | |
| B. | 元素周期表中的所有元素都是从自然界中发现的,过渡元素都是金属元素 | |
| C. | 非金属元素形成的共价化合物中,原子的最外层都达到了8电子的稳定结构 | |
| D. | 第ⅠA族与第ⅦA族元素间可形成共价化合物或离子化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 料酒可以除去食物中的腥味 | |
| B. | 裂化汽油可用于萃取碘水中的碘单质 | |
| C. | 葡萄糖可用于补钙药物的合成 | |
| D. | 次氯酸钠溶液可用于环境的消毒杀菌 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaF、NH4Cl | B. | NaOH、NaClO | C. | CaO、Na2O2 | D. | MgCl2、Mg(OH)2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验操作和现象 | 实验结论 |
| A | 在两支试管中分别加入已打磨的一小段镁条和一小块铝片,分别加入2mol•L-1盐酸2mL,发现镁条反应较剧烈 | 金属性:镁强于铝 |
| B | 滴有少量水的小木板上放上小烧杯,加入20gBa(OH)2•8H2O和10gNH4Cl,用玻璃棒快速搅拌并触摸烧杯外壁下部,发现很冷 | Ba(OH)2•8H2O与NH4Cl的反应为吸热反应 |
| C | 浸透石蜡的矿渣棉用喷灯加热,产生的气体通入酸性KMnO4溶液,溶液褪色 | 产生的气体中可能含乙烯、丙烯等烯烃 |
| D | 向5mL0.1mol•L-1 FeCl3溶液中滴入0.1mol•L-1KI溶液5~6滴,加2mLCCl4振荡,静置后取上层清液滴加KSCN溶液,溶液变红 | Fe3+与I-的反应有一定限度 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 如图为氢氧燃料电池装置示意图.
如图为氢氧燃料电池装置示意图.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 中和反应要吸收能量 | |
| B. | 化学反应中有物质变化也有能量变化 | |
| C. | 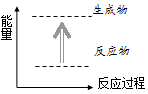 如图所示的反应为放热反应 | |
| D. | 化学键断裂放出能量,化学键生成吸收能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | MnCO3 | B. | MnO2 | C. | Na2CO3 | D. | 氨水 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com