
| A.CO2 | B.H3O+ | C.CH4 | D.[Ag(NH3)2] + |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:不详 题型:单选题
| A.一定是共价键 | B.一定是离子键 |
| C.可能是共价键,也可能是离子键 | D.上述说法都不正确 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.离子化合物中一定含有金属元素 |
| B.金属元素不可能存在于阴离子中 |
| C.含有非极性键的化合物不一定是共价化合物 |
| D.由两种元素构成的共价化合物分子中的化学键都是极性键 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.HCl KCl | B.CO2 SiO2 | C.NH4Cl CCl4 | D.NaOH Na2O2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
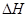 =-a kJ·mol-1 ② 2A → A-A;
=-a kJ·mol-1 ② 2A → A-A;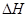 =-b kJ·mol-1
=-b kJ·mol-1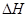 =-c kJ·mol-1
=-c kJ·mol-1 X(g);
X(g);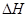 =-a KJ·mol-1(a>0,X为A、B、C三种元素组成的一种化合物)。初始投料与各容器达到平衡时的有关数据如下:
=-a KJ·mol-1(a>0,X为A、B、C三种元素组成的一种化合物)。初始投料与各容器达到平衡时的有关数据如下:| 实验 | 甲 | 乙 | 丙 |
| 初始投料 | 2 mol A2、1 mol BC | 1 mol X | 4 mol A2、2 mol BC |
| 平衡时n(X) | 0.5mol | n2 | n3 |
| 反应的能量变化 | 放出Q1kJ | 吸收Q2kJ | 放出Q3kJ |
| 体系的压强 | P1 | P2 | P3 |
| 反应物的转化率 | 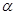 1 1 | 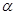 2 2 | 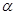 3 3 |
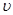 ( A2)为 。
( A2)为 。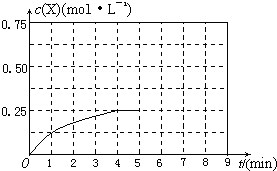
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.石墨的结构 | B.白磷的结构 | C.CCl4的结构 | D.立方烷(C8H8)的结构 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.①⑦ | B.①⑤⑦ | C.⑦ | D.②⑦ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
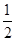 O2(g)=CO(g) ΔH=-Q1kJ·mol-1,C(s)+O2(g)=CO2(g) ΔH=-Q2 kJ·mol-1,有关上述反应的叙述错误的是( )
O2(g)=CO(g) ΔH=-Q1kJ·mol-1,C(s)+O2(g)=CO2(g) ΔH=-Q2 kJ·mol-1,有关上述反应的叙述错误的是( )| A.Q1<Q2 |
| B.生成物总能量均高于反应物总能量 |
| C.由1 mol C反应生成1 mol CO气体时放出Q1 kJ热量 |
| D.1 mol CO2气体具有的能量大于1 mol干冰具有的能量 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.干冰汽化时化学键发生断裂 |
| B.SiO2晶体有多种晶型,其基本结构单元是[SiO4]四面体结构 |
| C.Na2O和Na2O2所含化学键类型完全相同 |
| D.Br2蒸气被木炭吸附时共价键被破坏 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com