
A��B��C��D��E��F����Ԫ�ؾ�λ�����ڱ���ǰ�����ڣ���ԭ��������������Ԫ��A��ԭ�Ӱ뾶��С��Ԫ�أ�BԪ�ػ�̬ԭ�ӵĺ�����ӷ�ռ�ĸ�ԭ�ӹ�����ܼ�����DԪ��ԭ�ӵ��ѳɶԵ���������δ�ɶԵ���������3����E��D����ͬһ���壻Fλ��ds������ԭ�ӵ������ֻ��1�����ӡ�
��1��E+���ӵĵ����Ų�ʽ�� ��
��2��B��C��DԪ�صĵ�һ�������ɴ�С��˳���� ��
��3��B��CԪ�ص�ijЩ�⻯��ķ����о�����18�����ӣ���B�������⻯��Ļ�ѧʽ�� ��B��C����Щ�⻯��ķе����ϴ����Ҫԭ���� ��
��4��A��B��D���γɷ���ʽΪA2BD��ij�������û����������Bԭ�ӵĹ���ӻ������� ��1 mol�÷����к��Цм�����Ŀ�� ��
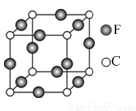
��5��C��E��Ԫ���γɵ�ij������ľ����ṹ��ͼ��ʾ����û�����Ļ�ѧʽ�� ��Cԭ�ӵ���λ���� ��
 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2017�콭��ʡ�����ϵ�һ�β��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
����������ȷ����
A�����Ҵ���CCl4������ȡ��ˮ�еĵⵥ��
B��CO2��SiO2�����ۻ�ʱ���˷����Ӽ���������������ͬ
C��PCl3��Na2O2�и�ԭ�ӻ���������㶼����8�����ȶ��ṹ
D��24Mg34S�����е�����������������֮��Ϊ1��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
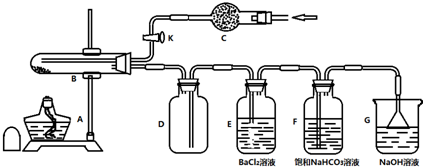
| �ζ�����ʵ������ | 1 | 2 | 3 |
| V����Ʒ��/mL | 20.00 | 20.00 | 20.00 |
| V��KMnO4��/mL���������� | 1.50 | 0.20 | 0.00 |
| V��KMnO4��/mL���ն����� | 19.85 | 20.22 | 19.98 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �Ҵ���Һ | B�� | �Ȼ�����Һ | C�� | ����������Һ | D�� | ������������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�콭��ʡ�����ϵ�һ�β��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
��ѧ����Դ������������������������ء�����˵������ȷ����
A��CO2�ͷ����������ʵĴ����ŷŻ��������ЧӦ�ļӾ�
B�������ù�ҵ���������Ķ�����̼����ȫ��������
C��������ܶೡ�ݵ����ʹ�÷Ǿ��象Ĥ���Գ������̫���ܣ����ֵ�̼����
D����K2FeO4����Cl2��������ˮ����ɱ���������ã��Ҳ����γ��°������ˮ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��״���£���2.24L Cl2����ˮ���ɵõ�HClO���ӵ���Ŀ��0.1NA | |
| B�� | NA��Fe��OH��3�������ӵ�����Ϊ107g | |
| C�� | 8.0gCu2S��CuO�Ļ�����к���ͭԭ����Ϊ0.1NA | |
| D�� | 2.3gNa��������ȫ��Ӧ����Ӧ��ת�Ƶĵ���������0.1NA��0.2NA֮�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���

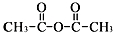
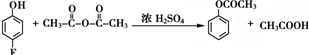 ��
��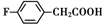 ��
��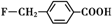
 ��������Ϊԭ���Ʊ�
��������Ϊԭ���Ʊ� �ĺϳ�·������ͼ�����Լ���ѡ�����ϳ�·������ͼʾ�����£�CH3COOH$��_{��}^{NaOH��Һ}$CH3CH2OH$��_{Ũ���ᣬ��}^{CH_{3}COOCH}$CH3COOCH2CH3��
�ĺϳ�·������ͼ�����Լ���ѡ�����ϳ�·������ͼʾ�����£�CH3COOH$��_{��}^{NaOH��Һ}$CH3CH2OH$��_{Ũ���ᣬ��}^{CH_{3}COOCH}$CH3COOCH2CH3���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
 ̫���ܵ�ذ���ϳ��������⣬����ͭ�������ء����Ȼ�ѧ���ʣ�
̫���ܵ�ذ���ϳ��������⣬����ͭ�������ء����Ȼ�ѧ���ʣ��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�콭��ʡ����и�����ѧ����������һ��ѧ�Ծ��������棩 ���ͣ�ѡ����
ͨ���Ҵ���ȡ����ͨ������������;����
a��CH3CH2OH(g)��H2O(g)��4H2(g)��2CO(g) ��H1��+256.6 kJ��mol��1
b��2CH3CH2OH(g)��O2(g)��6H2(g)��4CO(g) ��H2��+27.6 kJ��mol��1
������˵����ȷ����
A������a�ķ�Ӧ�¶ȣ��Ҵ���ת��������
B����b��֪���Ҵ���ȼ����Ϊ13.8 kJ��mol��1
C��2H2(g)��O2(g)��2H2O(g) ��H����485.6 kJ��mol��1
D����ȡ������������;��b���ĵ���������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com