
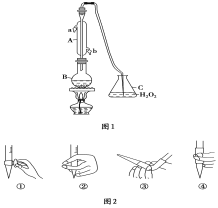
【题目】国家标准(GB27602011)规定葡萄酒中SO2最大使用量为0.25 g·L-1。某兴趣小组用题图1装置(夹持装置略)收集某葡萄酒中SO2,并对含量进行测定。
(1)图2中①的仪器名称 。
(2)B中加入300.00 mL葡萄酒和适量盐酸,加热使SO2全部逸出并与C中H2O2完全反应,其化学方程式为 。
(3)除去C中过量的H2O2,然后用0.090 0 mol·L-1 的NaOH标准溶液进行滴定,滴定前排气泡时,应选择图2中的________;若滴定终点时溶液的pH=8.8,则选择的指示剂为________;滴定的终点现象 ;若用50 mL滴定管进行实验,当滴定管中的液面在刻度“10”处,则管内液体的体积 (填序号)___________(①=10 mL,②=40 mL,③<10 mL,④>40 mL)。
(4)滴定至终点时,消耗NaOH溶液25.00 mL,该葡萄酒中SO2含量为:___________g·L-1。
(5)该测定结果比实际值偏高,分析原因并利用现有装置提出改进措施______________________。
【答案】(1)酸式滴定管 (2)SO2+H2O2===H2SO4
(3)③ 酚酞 滴入最后一滴溶液,锥形瓶溶液由无色变为浅红色且半分钟不褪色 ④
(4)0.24(5)原因:盐酸的挥发;改进措施:用不挥发的强酸如硫酸代替盐酸,或用蒸馏水代替葡萄酒进行对比实验,排除盐酸挥发的影响
【解析】
试题分析:(1)图2中①的仪器名称为酸式滴定管;
(2)双氧水具有氧化性,能够将二氧化硫氧化成硫酸,反应的化学方程式为:SO2+H2O2=H2SO4;
(3)氢氧化钠溶液为碱性溶液,应该使用碱式滴定管,碱式滴定管中排气泡的方法:把滴定管的胶头部分稍微向上弯曲,再排气泡,所以排除碱式滴定管中的空气用③的方法;滴定终点时溶液的pH=8.8,应该选择酚酞做指示剂(酚酞的变色范围是8.2~10.0),且可根据滴入最后一滴溶液,锥形瓶溶液由无色变为浅红色且半分钟不褪色判断滴定终点;若用50mL滴定管进行实验,当滴定管中的液面在刻度“10”处,滴定管的0刻度在上方,10mL刻度线下方还有40mL有刻度的溶液,另外滴定管50mL刻度线下有液体,因此管内的液体体积>(50.00mL-10.00mL)=40.00mL,所以④正确;
(4)根据2NaOH~H2SO4~SO2可知SO2的质量为:1/2×(0.0900mol/L×0.025L)×64g/mol=0.072g,该葡萄酒中的二氧化硫含量为:0.0372g÷0.3L=0.24g/L;
(5)由于盐酸是挥发性酸,挥发的酸消耗氢氧化钠,使得消耗的氢氧化钠溶液体积增大,测定结果偏高;因此改进的措施为:用不挥发的强酸,如硫酸代替盐酸,或用蒸馏水代替葡萄酒进行对比实验,扣除盐酸挥发的影响。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】碳是形成化合物种类最多的元素,其单质及化合物有独特的性质和用途。请回答下列问题。
(1)碳原子核外电子有_____种不同的运动状态。碳原子的价电子在形成sp3杂化后,其轨道表达式为_____。
(2)写出一种CO32-的等电子体微粒的化学式_______,其空问构型为_______。
(3)有机物M(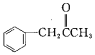 )在一定条件下生成N(
)在一定条件下生成N(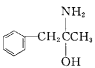 )。
)。
①沸点:M_____N (填“大于”或“小于”)。
②M中碳原子杂化类型为_____,不同杂化类型的碳原子数之比为_____。
③有机物N中除氢原子之外的其他原子的第一电离能由大到小的顺序为_____。
(4)已知CaCO3的热分解温度为900℃,SrCO3的热分解温度为1172℃,试从原子结构的角度解释CaCO3的热分解翻度低于SrCO3的原因_____________。
(5)石墨是碳的一种同素异形体,它的一种晶胞结构和部分晶胞参数如下图:
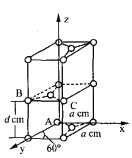
①原子坐标参数描述的是晶胞内原子间的相对位置。石墨晶胞中碳原子A、B的坐标参数分别为:A(0,0,0)、B(0,1,1/2)。则C原子的坐标参数为_______________。
②晶胞参数用以描述晶胞的大小和形状。已知石墨晶胞底边长为am ,层间距为dcm,阿伏加德罗常数的值为NA,则石墨的密度为_____g·cm-3(写出表达式即可)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有机物命名及其一氯代物的同分异构体数目正确的是( )
命名 | 一氯代物 | |
A | 2-甲基-2-乙基丙烷 | 4 |
B | 1,3-二甲基苯 | 3 |
C | 2,2,3-三甲基戊烷 | 6 |
D | 2,3-二甲基-4-乙基己烷 | 7 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NH4Al(SO4)2是食品加工中最为快捷的食品添加剂,用于焙烤食品;NH4HSO4在分析试剂、医药、电子工业中用途广泛。请回答下列问题:
(1)NH4Al(SO4)2可作净水剂,其原理是____________________ (用离子方程式说明)。
(2)相同条件下,0.1 mol·L-1 NH4Al(SO4)2 溶液中 c(NH4+)________(填“等于”、“大于”或“小于”) 0.1 mol·L-1 NH4HSO4溶液中 c(NH4+)。
(3)均为 0.1 mol·L-1 的几种电解质溶液的pH 随温度变化的曲线如图1所示。
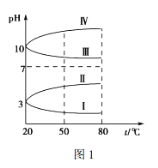
①其中符合0.1 mol·L-1 NH4Al(SO4)2溶液的pH随温度变化的曲线是________(填罗马数字),导致 NH4Al(SO4)2溶液的pH 随温度变化的原因是___________ 。
②20 ℃时,0.1 mol·L-1 NH4Al(SO4)2溶液中 2c(SO42-)-c(NH4+)-3c(Al3+)=___________mol·L-1。
(4)室温时,向100 mL 0.1 mol/L的NH4HSO4溶液中滴加 0.1 mol/L的NaOH溶液,当加入NaOH溶液的体积分别为以下数据时:a、100ml b、150ml c、200ml。分析 a、b、c三种混合溶液中,水的电离程度最大的是______填(“a”、“b”或“c”);当加入NaOH溶液使溶液呈中性时,溶液中各离子浓度由大到小的排列顺序是_____ __ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对可逆反应4NH3(g)+ 5O2(g)![]() 4NO(g)+ 6H2O(g),下列叙述正确的是( )
4NO(g)+ 6H2O(g),下列叙述正确的是( )
A. 达到化学平衡时,4υ正(O2)= 5υ逆(NO)
B. 若单位时间内生成x mol NO的同时,消耗x mol NH3 ,则反应达到平衡状态
C. 达到化学平衡时,若增加容器体积,则正反应速率减少,逆反应速率增大
D. 化学反应速率关系是:2υ正(NH3)= 3υ正(H2O)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)纯碱溶液中滴入酚酞溶液,观察到的现象是 ;原因是 。(用离子方程式说明)
(2)把AlCl3溶液蒸干灼烧,最后得到的主要固体产物是 ,为什么?(用化学方程式和必要的文字说明) 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是实验室制备1,2—二溴乙烷并进行一系列相关实验的装置(加热及夹持设备已略)。
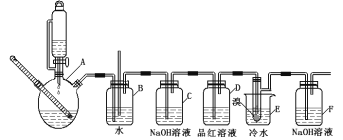
已知: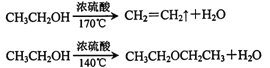
相关数据列表如下:
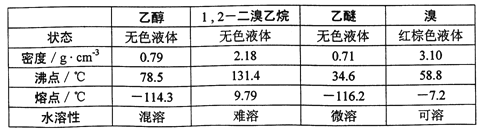
请完成下列填空:
(1)实验中应迅速将温度升高到170℃左右的原因是
(2)气体发生装置使用连通滴液漏斗的原因_________________________
(3)安全瓶B在实验中有多重作用,其一可以检查实验进行中B后面的装置中导管是否发生堵塞,请写出发生堵塞时瓶B中的现象 ;
(4)装置D中品红溶液的作用是_______________________;
(5)容器C、F中都盛有NaOH溶液,F中NaOH溶液的作用是 ;
(6)反应过程中用冷水冷却装置E不能过度冷却(如用冰水),其原因是__________________。
(7)某学生在做此实验时,使用一定量的液溴,当溴全部褪色时,所消耗乙醇和浓硫酸混合液的量,比正常情况下超过许多,如果装置的气密性没有问题,试分析可能的原因 ;(写出两条即可)
(8)除去产物中少量未反应的Br2后,还含有的主要杂质为 ,要进一步提纯,下列操作中必须用到的是 (填入正确选项前的字母);
A.重结晶 B.过滤 C.萃取 D.蒸馏
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com