
A、B、C、D、E都是短周期元素,原子序数依次增大,元素B的原子价电子构型为ns2npn+2 。B、C同周期, C为周期表中电负性最大的元素,A、D同主族。A、B能形成两种液态化合物甲和乙,原子个数比分别为2∶1和1∶1,E 是地壳中含量最高的金属元素。根据以上信息回答下列问题:
⑴写出A、B、C、D、E元素符号___、___、___、___、___、
⑵B原子的电子排布图为_________________。D离子的电子排布式为______________________,甲、乙两分子中含有非极性共价键的物质的电子式是___________________,
⑶DBA中的化学键类型为____________、____________属于 化合物(填“离子”或“共价”)
⑷A的硫化物中,A原子以 杂化轨道成键,分子空间构型为 ;
(5)分别写出DBA水溶液与E、DBA与E的氧化物反应的化学方程式.
_____ ______ _______
_______ ______ _______ __
科目:高中化学 来源: 题型:
N2H4是一种高效清洁的火箭燃料。0.25 mol N2H4(g)完全燃烧生成氮气和气态水时,放出133.5 kJ热量。则下列热化学方程式中正确的是
A. N2H4+
N2H4+ O2===
O2=== N2+H2O ΔH=-267 kJ·mol-1
N2+H2O ΔH=-267 kJ·mol-1
B.N2H4(g)+O2(g)===N2(g)+2H2O(l) ΔH=-133.5 kJ·mol-1
C.N2H4(g)+O2(g)===N2(g)+2H2O(g) ΔH=+534 kJ
D.N2H4(g)+O2(g)===N2(g)+2H2O(g) ΔH=-534 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA为阿伏加德罗常数的值。下列说法正确的是
A.标准状况下,2.24L苯中含有的C-H键的数目为0.6NA
B.标准状况下,由H2O2分解制得4.48LO2转移的电子数目为0.8NA
C.14 g 由乙烯与环丙烷(C3H6)组成的混合气体含有的碳原子数目为NA
D.常温下,1 L pH=2的H2SO4溶液中含有的H+数目为0.02NA
查看答案和解析>>
科目:高中化学 来源: 题型:
若不断地升高温度,实现“雪花―→水―→水蒸气―→氧气和氢气”的变化。在变化的各阶段被破坏的微粒间的相互作用依次是 ( )
A.氢键;分子间作用力;非极性键 B.氢键;分子间作用力;极性键
C.氢键;极性键;分子间作用力 D.分子间作用力;氢键;非极性键
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于范德华力的叙述中,正确的是( )
A.范德华力的实质也是一种电性作用,所以范德华力是一种特殊化学键
B.任何分子间在任意情况下都会产生范德华力
C.范德华力与化学键的区别是作用力的强弱问题
D.范德华力非常微弱,故破坏范德华力不需要消耗能量
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述中正确的是( )
A.含有共价键的化合物一定是共价化合物 B.含有离子键的化合物一定是离子化合物
C.含非极性键的纯净物一定是单质 D.原子最外层2个电子的元素一定在ⅡA族
查看答案和解析>>
科目:高中化学 来源: 题型:
苯和乙烯相比较,下列叙述中正确的是( )
A.都易与溴发生取代反应
B.都易发生加成反应
C.乙烯易发生加成反应,苯不能发生加成反应
D.乙烯易被酸性高锰酸钾溶液氧化,苯不能被酸性高锰酸钾溶液氧化
查看答案和解析>>
科目:高中化学 来源: 题型:
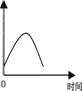
把镁条投入到盛有盐酸的敞口容器中,产生H2的速率速率
可由右上图表示。在下列因素中对产生H2速率有影响的是
①盐酸的浓度 ②镁条的表面积 ③溶液的温度 ④Cl-的浓度
A.①④ B.③④ C.①②③ D.②③
查看答案和解析>>
科目:高中化学 来源: 题型:
500 mL KNO3和Cu(NO3)2的混合溶液中c(NO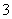 )=0.6 mol·L-1,用石墨作电极电解此溶液,当通电一段时间后,两极均收集到2.24 L气体(标准状况下),假定电解后溶液体积仍为500 mL,下列说法正确的是 ( )
)=0.6 mol·L-1,用石墨作电极电解此溶液,当通电一段时间后,两极均收集到2.24 L气体(标准状况下),假定电解后溶液体积仍为500 mL,下列说法正确的是 ( )
A.原混合溶液中c(K+)为0.2 mol·L-1
B.上述电解过程中共转移0.2 mol电子
C.电解得到的Cu的物质的量为0.05 mol
D.电解后溶液中c(H+)为0.2 mol·L-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com