
| A、A、B、C的浓度不再变化 |
| B、混合气体的总物质的量不再变化 |
| C、单位时间内a mol A生成,同时生成3a mol B |
| D、C的生成速率与C的分解速率相等 |


科目:高中化学 来源: 题型:
| A、64g氧气中含氧分子数为2NA |
| B、1.7gOH-中所含的电子数为NA |
| C、49g硫酸中所含氧原子数为2NA |
| D、58.5g氯化钠中所含的离子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
 我校环保兴趣小组在处理污水样品时,需用质量分数为37%的浓盐酸(密度为1.19g/cm3)配制成250mL 0.1mol?L-1的盐酸溶液.
我校环保兴趣小组在处理污水样品时,需用质量分数为37%的浓盐酸(密度为1.19g/cm3)配制成250mL 0.1mol?L-1的盐酸溶液.查看答案和解析>>
科目:高中化学 来源: 题型:
| 催化剂 |
| 加热、加压 |
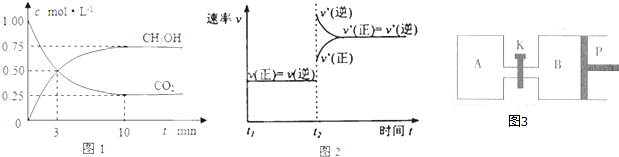
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①③ | B、②③④ |
| C、③⑤ | D、③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、降低温度 |
| B、缩小体积 |
| C、减小压强 |
| D、增大H2浓度 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 9a+b |
| 3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、同温同压下,H2(g)+Cl2(g)═2HCl(g)在光照和点燃条件下的△H不同 |
| B、反应:CH2=CH2+H2→CH3-CH3;△H<O,使用和未使用催化剂时,反应热不同 |
| C、用硝酸这一种试剂就能将MgI2、AgNO3、Na2CO3、NaAlO2四种溶液鉴别出来 |
| D、依据丁达尔现象就可将分散系分为溶液、胶体与浊液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com