
| A. | ①② | B. | ②④ | C. | ③④ | D. | ②③ |
分析 ①氯气会和乙烷之间发生取代反应;
②饱和碳酸钠溶液可以和乙酸之间发生中和反应;
③二氧化碳与碳酸反应生成碳酸氢钠;
④乙酸与生石灰反应,而乙醇不能.
解答 解:①光照条件下通入Cl2,氯气会和乙烷之间发生取代反应,和乙烯之间发生加成反应,这样即将杂质除去,又将要留的物质反应了,不符合除杂的原则,故①错误;
②饱和碳酸钠溶液可以和乙酸之间发生中和反应,甲醛易挥发,蒸馏即可分离,故②正确;
③二氧化碳与碳酸钠反应生成碳酸氢钠,二氧化硫与碳酸钠反应生成生成亚硫酸钠,水和二氧化碳,将原物质除掉了,不符合除杂原则,故③错误;
④乙酸与生石灰反应,而乙醇不能,且乙醇易挥发,而乙酸钙为离子型化合物,沸点高,故除去乙醇中少量的乙酸可以加足量生石灰后蒸馏,故④正确;
故选B.
点评 本题考查物质的分离与除杂,难度不大,解决除杂问题时,抓住除杂质的必需条件(加入的试剂只与杂质反应,反应后不能引入新的杂质)是正确解题的关键.


 教材全解字词句篇系列答案
教材全解字词句篇系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
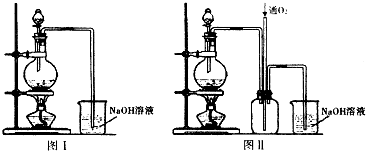
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向硫酸铝溶液中滴加过量的氨水:Al3++4OH?═AlO2?+2H2O | |
| B. | 金属铜与浓硝酸反应:3Cu+8H++2NO3?═3Cu2++2NO↑+4H2O | |
| C. | 实验室用浓盐酸与MnO2反应制Cl2:MnO2+2H++2Cl?$\frac{\underline{\;\;△\;\;}}{\;}$Cl2↑+Mn2++H2O | |
| D. | 向NaAlO2溶液中通入过量CO2:AlO2-+CO2+2H2O=Al(OH)3↓+HCO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 (1)实事证明,能设计成原电池的反应通常是放热反应,下列化学反应在实际中可以设计成原电池的是C
(1)实事证明,能设计成原电池的反应通常是放热反应,下列化学反应在实际中可以设计成原电池的是C查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 容量瓶用蒸馏水洗净后需晾干才能使用 | |
| B. | 需称取NaC1O固体144g | |
| C. | 所配得NaC1O消毒液久置后会失效 | |
| D. | 8 4消毒液的消毒原理是利用了NaClO的强碱性 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com