
 ,乙是过氧化钠,过氧化钠中钠离子和过氧根离子之间存在离子键,氧原子和氧原子之间存在共价键,
,乙是过氧化钠,过氧化钠中钠离子和过氧根离子之间存在离子键,氧原子和氧原子之间存在共价键, ;离子键、共价键;
;离子键、共价键;
| ||
| 冰晶石 |
| ||
| 冰晶石 |


 举一反三同步巧讲精练系列答案
举一反三同步巧讲精练系列答案 口算与应用题卡系列答案
口算与应用题卡系列答案科目:高中化学 来源: 题型:
| A、1.0mol/L的NaHSO4溶液:K+、Fe2+、NO3-、Cl- | ||
| B、l.0mol?L-1 NaClO溶液:Fe2+、K+、I-、Cl- | ||
| C、甲基橙显黄色的溶液:Na+、CO32-、NO3-、SO32- | ||
D、在
|
查看答案和解析>>
科目:高中化学 来源: 题型:
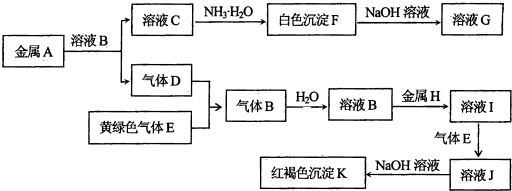
查看答案和解析>>
科目:高中化学 来源: 题型:
压强/MPa 体积分数/% 温度/℃ |
1.0 | 2.0 | 3.0 |
| 810 | 54.0 | a | b |
| 915 | c | 75.0 | d |
| 1000 | e | f | 83.0 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 工业制硝酸的主要反应为:
工业制硝酸的主要反应为:| 浓度 | c(NH3)(mol/L) | c(O2)(mol/L) | c(NO)(mol/L) |
| 时间 | |||
| 起始 | 0.8 | 1.6 | 0 |
| 第2min | 0.6 | a | 0.2 |
| 第4min | 0.3 | 0.975 | 0.5 |
| 第6min | 0.3 | 0.975 | 0.5 |
| 第8min | 0.7 | 1.475 | 0.1 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:

| A、图l用于制取纯净的NO2气体 |
| B、图2用于研究温度对化学平衡的影响 |
| C、图3用于实验室Cl2的收集 |
| D、图4用于除去CO2气体中的HCl杂质 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na+、Fe2+、MnO4-、NO3- |
| B、Al3+、NH4+、Br-、OH- |
| C、Na+、K+、SO42-、ClO- |
| D、K+、Ca2+、NO3-、CO32- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com