
(1)在常温下,0.5mol甲醇在氧气中完全燃烧生成CO2和液态水,放出热量363.3kJ.写出该反应的热化学方程式: _________________________
(2)请设计一个燃料电池:电解质为强碱溶液,Pt作电极,在电极上分别通入甲醇和氧气。通入甲醇的电极应为 极(填“正”或“负”),该电极上发生的电极反应式为 。
(3)用Pt电极电解盛有1L pH=6的硝酸银溶液,如图甲所示,则右边电极上发生的电极反应式为 .
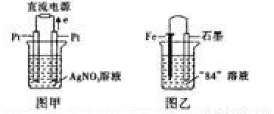
(4)某化学学习兴趣小组为了研究金属的腐蚀现象,将一枚铁钉放在“84”消毒液(NaClO)中,某同学设计了如图乙所示实验装置,写出石墨极上发生的电极反应式:
(1)CH3OH(l)+3/2O2(g)==CO2(g)+2H2O(l);△H=-726.6KJ·mol-1(3分)
(2)负(1分) CH3OH+8OH--6e-==CO32-+6H2O(3分)
(3)4OH--4e-==2H2O+O2↑或2H2O-4e-==O2↑+4H+(2分)
(4)ClO-+H2O+2e-==Cl-+2OH-(2分)
【解析】
试题分析:(1)在热化学方程式中物质的计量系数表示的是物质的量,故0.5mol甲醇在氧气中完全燃烧生成CO2和液态水,放出热量363.3kJ则1mol甲醇在氧气中完全燃烧生成CO2和液态水,放出热量726.6KJ,其热化学方程式为:
CH3OH(l)+3/2O2(g)==CO2(g)+2H2O(l);△H=-726.6KJ·mol-1; (2)、燃料为负极,在强碱性溶液中甲醇的氧化产物应为碳酸盐,故电极上发生的电极反应为: CH3OH+8OH--6e-==CO32-+6H2O;(3)用惰性电极电解硝酸银溶液时阳极是氢氧根离子失电子产生氧气,也可以写成水失去电子产生氧气,剩余H+;(4)此装装置构成了原电池,ClO-具有氧化性,正极上得电子生成Cl-。
考点:热化学方程式的书写,原电池原理的应用


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2015届安徽省高二上学期期中考试化学试卷(解析版) 题型:选择题
两种气态烃组成的混合气体,完全燃烧后得到CO2和H2O的物质的量随着混合烃物质的量的变化如图所示,则下列对混合烃的判断正确的是
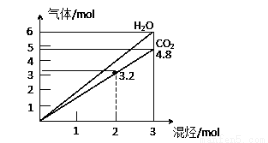
①可能有C2H2 ②一定有CH4 ③一定有C3H8 ④一定没有C2H6 ⑤可能有C2H6
A.②④ B.②⑤ C.③④ D.②③
查看答案和解析>>
科目:高中化学 来源:2015届安徽省高一上学期期中考试化学试卷(解析版) 题型:选择题
在无色透明强酸性溶液中,能大量共存的离子组是
A.K+、Cu2+、NO3﹣、SO42﹣ B.K+、Na+、Cl﹣、CO32﹣
C.Zn2+、NH4+、NO3﹣、Cl﹣ D.K+、Na+、MnO4﹣、SO42﹣
查看答案和解析>>
科目:高中化学 来源:2015届安徽省铜陵市高三上学期第二次月考化学试卷(解析版) 题型:选择题
在允许加热的条件下,只用一种试剂就可以鉴别(NH4)2SO4、KCl、MgCl2、Al2(SO4)3和Fe2(SO4)3溶液,这种试剂是 ( )
A.NaOH B.NH3·H2O
C.AgNO3 D.BaCl2
查看答案和解析>>
科目:高中化学 来源:2015届安徽省铜陵市高三上学期第二次月考化学试卷(解析版) 题型:选择题
下列叙述正确的是 ( )
A.为提醒人们在使用浓H2SO4时要注意安全,贮存浓H2SO4的容器上贴有下图标识

B.实验室可通过蒸馏的方法除去自来水中含有的Cl-等杂质制蒸馏水
C.做焰色反应实验时,应先将铂丝(或铁丝)用稀硫酸洗净后,在酒精灯外焰上灼烧至没有颜色时,再蘸取待检溶液进行实验
D.由于碱金属单质化学性质活泼,实验室中的各种碱金属单质均保存在煤油中
查看答案和解析>>
科目:高中化学 来源:2015届安徽省高三第一次联考化学试卷(解析版) 题型:选择题
常温下,取浓度均为0.05mol·L-1的弱酸HA溶液和氨水溶液各20mL,分别用0.05mol·L-1NaOH溶液、0.05mol·L-1盐酸进行中和滴定,滴定过程中pH随滴加溶液的体积变化关系如下图所示,下列说法正确的是( )
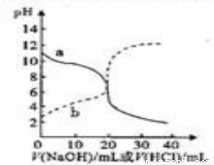
A.曲线a:滴加溶液到10mL时:c(A-)>c(Na+)>c(H+)>c(OH-)
B.曲线a:滴加溶液到20mL时:c(Cl-)>c(NH4+)>c(OH-)>c(H+)
C.曲线b:滴加溶液到10mL~20mL之间存在:c(NH4+)=c(Cl-)>c(OH-)=c(H+)
D.曲线b:滴加溶液到20mL时:c(Na+)=c(A-)+c(HA)
查看答案和解析>>
科目:高中化学 来源:2015届安徽省高三第一次联考化学试卷(解析版) 题型:选择题
向某种含AlCl3的混合溶液中逐滴加入NaOH溶液,其中生成某白色沉淀的量随NaOH加入量的变化关系如图所示。则下列离子组在你对应的溶液中可能大量共存的是( )
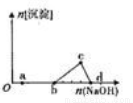
A. a点对应的溶液中:K+、Fe3+、SO42-、Cl-
B.b点对应的溶液中:Na+、S2-、NO3-、Cl-
C.c点对应的溶液中:K+、Ag+、NO3-、SO42-
D.d点对应的溶液中:K+、Mg2+、I-、CO32-
查看答案和解析>>
科目:高中化学 来源:2015届安徽省皖南八校高三第一次联考化学试卷(解析版) 题型:选择题
根据下列实验操作和现象,结论正确的是
| 操作 | 实验现象 | 结论 |
A | 向某溶液中加入氯化钡、稀硝酸的混合液 | 产生白色沉淀 | 该溶液中一定含有SO42-或SO32- |
B | 将某气体通入品红溶液 | 溶液红色褪去 | 该气体一定SO2 |
C | 把湿润的碘化钾——淀粉试纸放入某一红棕色的气体中 | 试纸变蓝色 | 该气体可能是NO2 |
D | 将通入SO2到酸性高锰酸钾溶液中 | 溶液紫色褪去 | SO2具有漂白性 |
查看答案和解析>>
科目:高中化学 来源:2015届宁夏银川市高三上学期期中考试化学试卷(解析版) 题型:选择题
有四种物质:NaHCO3溶液、NaOH溶液、盐酸、铁粉。它们两两之间发生的反应最多
A.3个 B.4个 C.5个 D.6个
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com