
| A. | 碳酸钙受热分解 | B. | 乙醇燃烧 | ||
| C. | 盐酸与氢氧化钠中和 | D. | 氧化钙溶于水 |
分析 生成物总能量高于反应物总能量的反应属于吸热反应,根据常见的放热反应和吸热反应进行判断.若反应物的总能量大于生成物的总能量则为放热反应.
常见的放热反应有:所有的物质燃烧、所有金属与酸、所有中和反应、绝大多数化合反应,铝热反应;
常见的吸热反应有:个别的化合反应(如C和CO2)、绝大数分解反应、少数分解置换以及某些复分解(如铵盐和强碱).
解答 解:A.碳酸钙受热分解属于吸热反应,生成物总能量高于反应物总能量,故A正确;
B.乙醇燃烧属于放热反应,生成物的总能量小于反应物的总能量,故B错误;
C.盐酸与氢氧化钠中和反应属于放热反应,生成物的总能量小于反应物的总能量,故C错误;
D.氧化钙溶于水与水发生化合反应,属于放热反应,生成物的总能量小于反应物的总能量,故D错误.
故选A.
点评 本题主要考查了放热反应和放热反应,题目难度不大,掌握常见的放热反应和放热反应是解题的关键.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 $\stackrel{Br_{2}/P}{→}$
$\stackrel{Br_{2}/P}{→}$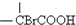
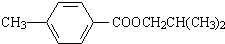 .
.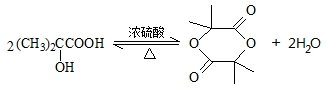 ,该反应属于酯化反应(填反应类型).
,该反应属于酯化反应(填反应类型).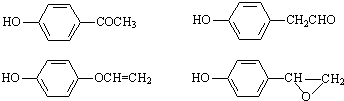 .
. )结构.
)结构.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NO2、BF3、NCl3分子中没有一个分子中原子的最外层电子都满足了8电子稳定结构 | |
| B. | P4和CH4都是正四面体分子且键角都为109°28′ | |
| C. | NaCl晶体中与每个Na+距离相等且最近的Na+共有8个 | |
| D. | 区分晶体和非晶体最科学的方法是对固体进行X一射线衍射实验 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 可用电解饱和的MgCl2溶液的方法获得金属镁 | |
| B. | 电解CuSO4溶液精炼金属铜时,用铁做阳极 | |
| C. | 电解熔融Al2O3方法冶炼金属铝时,同时要加入冰晶石作助熔剂 | |
| D. | 工业上常采用活泼金属还原法冶炼金属银 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验步骤 | 实验现象 | 结论 |
| 取适量样品加热浓缩后加入试管中,再加入适量硫酸和铜片,加热. | 假设1成立 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com