
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案科目:高中化学 来源:不详 题型:单选题
| A.b>a>c | B.a=b=c | C.c>a>b | D.b>c>a |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.1×10-7mol?L-1 | B.1×10-12mol?L-1 |
| C.1×10-2mol?L-1 | D.1×10-14mol?L-1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.无论是纯水还是稀溶液,在室温下其[H+]?[OH-]=1×10-14mol2?L-2 |
| B.[H+]等于1×10-7mol/L的溶液一定是中性溶液 |
| C.0.2mol/LCH3COOH溶液中的[H+]是0.1mol/LCH3COOH溶液中的[H+]的2倍 |
| D.任何浓度的溶液都可以用pH来表示其酸性的强弱 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.将水加热,Kw增大,pH不变 |
| B.向水中加入少量NaHSO4固体,c(H+)增大,Kw不变 |
| C.向水中加入少量NaOH固体,平衡逆向移动,c(OH-)降低 |
| D.向水中加入少量NH4Cl固体,平衡正向移动,c(OH-)增大 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
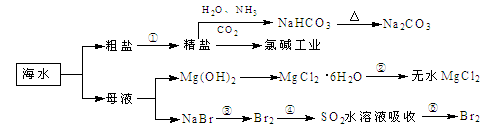
| A.过程①中除去粗盐中的SO、Ca2+、Mg2+、Fe3+等杂质,加入的药品顺序为:Na2CO3溶液→NaOH溶液→BaCl2溶液→过滤后加盐酸 |
| B.用澄清的石灰水可鉴别NaHCO3和Na2CO3 |
| C.过程②中结晶出的MgCl2·6H2O要在HCl氛围中加热脱水制得无水MgCl2 |
| D.工业上通过电解饱和MgCl2溶液制取金属镁 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com