
【题目】下列金属用热还原法冶炼的是( )
A. 钠 B. 银 C. 铁 D. 汞
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】在一个密闭容器中,中间有一个可自由滑动的隔板,将容器分成两部分。当左边充入1molN2,右边充入8gCO和CO2的混合气体时,隔板处于如下图所示位置,V甲:V乙=4:1(两侧温度、压强均相同)。则混合气体中CO和CO2的物质的量比为( )

A. 1:1 B. 1:3 C. 3:1 D. 2:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有一铁的氧化物样品,用50mL5mol/L的盐酸恰好完全溶解,所得溶液还能与通入的0.56L氯气(标准状况)反应,使Fe2+全部转化为Fe3+,则此氧化物为
A. Fe2O3 B. Fe3O4 C. Fe4O5 D. Fe5O7
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)现有下列十种物质:①蔗糖②熔融NaCl③石墨④铜丝⑤NaOH固体⑥SO2⑦NaHSO4固体⑧K2O固体⑨液态H2SO4⑩饱和FeCl3溶液 上述物质中可导电的是________(填序号,下同);上述物质中不能导电,但属于电解质的是_______________________。
(2)NaHSO4是一种酸式盐,请填写下列空白:
①NaHSO4晶体熔化时的电离方程式为______________________________。
②3 mol·L-1 NaHSO4与2 mol·L-1 Ba(OH)2溶液等体积混合,该反应总的离子方程为___________。
(3)实验室制备少量Fe(OH)3胶体所用的物质有__________(填序号),反应的离子方程式为________________________________________________。
(4)某强酸性反应体系中,反应物和生成物共六种物质:O2、MnO4-、H2O、Mn2+、H2O2、H+,已知该反应中H2O2只发生了如下过程:H2O2→O2。写出该反应的离子方程式:_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有机物的除杂方法正确的是(括号中的是杂质)
A. 乙酸(乙醛):加入新制的氢氧化铜悬浊液,加热
B. 苯(苯酚):加入溴水,过滤
C. 溴乙烷(溴单质):加入热氢氧化钠溶液洗涤,分液
D. 乙酸乙酯(乙酸):加入饱和碳酸钠溶液洗涤,分液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室里需要纯净的NaCl溶液,但手边只有混有Na2SO4、NH4HCO3的NaCl。某学生设计了如图所示方案提取纯净的NaCl溶液。(已知:NH4HCO3=NH3↑+CO2↑+H2O)

(1)操作②为什么不用硝酸钡溶液,其理由是_______________________________;
(2)进行操作②后,如何判断SO42-已除尽,方法是___________________________;
(3)操作③的目的是____________,其中涉及到的离子方程式是_______________;
(4)往滤液中加入盐酸的离子方程式是__________________________________;
(5)NH4HCO3在水溶液中的电离方程式_________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学设计了种用电解法制取Fe(OH)2的实验装置如图。通电后,溶液中产生白色沉淀,且较长时间不变色。下列说法中正确的是

A. 电源中"a"为正极," b"为负极
B. 电解池中的电解液可以是NaOH溶液但不能是NaCl溶液
C. A、B两端都必须使用铁作电极
D. B电极发生的反应:2H2O+2e-=H2↑+2OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用惰性电极电解下列溶液,一段时间后,加入一定质量的另一种物质(中括号内),溶液能与原来溶液完全一样的是( )
A. CuCl2[CuSO4] B. NaOH[NaOH] C. CuSO4[Cu(OH)2] D. NaCl[HCl]
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2SO2(g) +O2(g)=2SO3(g)反应过程的能量变化如图所示。已知1mol SO2(g)氧化为1mol SO3(g)的△H=-99KJ/mol。请回答下列问题:
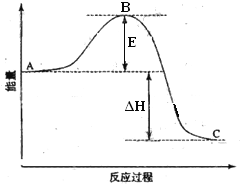
①图中A、C分别表示________、_______;
②E表示________;E的大小对该反应的反应热____(填“有”或“无”)影响。
③该反应通常用V2O5作催化剂,加V2O5会使图△H______(填“变大”、“变小”或“不变”),图中△H =______KJ/mol;
④已知单质硫的燃烧热为296 KJ/mol,计算由S(s)生成3molSO3(g)的△H=________KJ/mol。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com