

科目:高中化学 来源: 题型:
铝士矿(主要成分为![]() 、
、![]() 、
、![]() )是提取氧化铝的原料.提取氧化铝的
)是提取氧化铝的原料.提取氧化铝的
工艺流程如下:
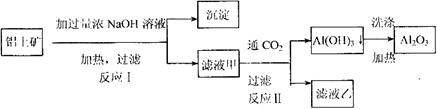
(1)写出反应Ⅱ的离子方程式_________________________________________________
(2)已知滤液乙的成分除![]() 外还含有
外还含有![]() 、
、![]() 中的一种或两种,所含物质的质量分数都在5%以上。请设计合理实验探究该滤液乙中
中的一种或两种,所含物质的质量分数都在5%以上。请设计合理实验探究该滤液乙中![]() 、
、![]() 的存在。仅限选择的仪器和试剂:烧杯、试管、带导管的橡皮塞、玻璃棒、蒸发皿、泥三角、三脚架、铁架台、酒精灯、过滤器、洗气瓶、滴管、药匙;lmol?L
的存在。仅限选择的仪器和试剂:烧杯、试管、带导管的橡皮塞、玻璃棒、蒸发皿、泥三角、三脚架、铁架台、酒精灯、过滤器、洗气瓶、滴管、药匙;lmol?L![]() 盐酸、2mol?L
盐酸、2mol?L![]() MgCl2溶液、澄清饱和石灰水。
MgCl2溶液、澄清饱和石灰水。
完成以下实验探究过程:
①提出假设:
假设1:滤液乙中除![]() 外还含有__________________;
外还含有__________________;
假设2:滤液乙中除![]() 外还含有_________________;
外还含有_________________;
假设3:滤液乙中除![]() 外还含有
外还含有![]() 、
、![]() ;
;
②设计实验方案:基于假设3,设计出实验方案(筒述实验操作、预期现象和结论)。
___________________________________________________________________________
__________________________________________________________________________。
(3)取滤液甲少许,加入过量盐酸,过滤;再用惰性电极电解其滤液,两极均有气体产生,且全部逸出,在阴极区还有沉淀生成,最后沉淀消失。沉淀消失的原因可用离子方程式表示为_____________________________________________________________
 (4)取(3)电解以后的溶液10.0 mL,经分析,该溶液中只含有两种等物质的量浓度的碱性溶质,向其中逐滴加入0.100 mol?L
(4)取(3)电解以后的溶液10.0 mL,经分析,该溶液中只含有两种等物质的量浓度的碱性溶质,向其中逐滴加入0.100 mol?L![]() 盐酸溶液,当加入50.0mL盐酸溶液时,生成的沉淀恰好溶解。
盐酸溶液,当加入50.0mL盐酸溶液时,生成的沉淀恰好溶解。
①加入50.0mL盐酸溶液发生
的离子反应按先后顺序依次为
__________________________
__________________________。
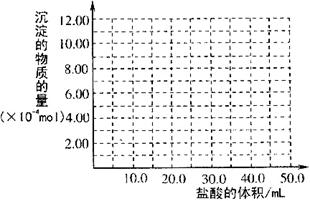
②请画出生成沉淀的物质的量
与加入盐酸体积的关系图。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com