
(14��) NaNO2����ۺ�ʳ�����ƣ�������ζ������ʹ����ʳ�ж�����֪NaNO2�ܷ������·�Ӧ��2NaNO2��4HI===2NO����I2��2NaI��2H2O��
��1��������Ӧ����������________��
��2������������Ӧ������NaNO2��NaCl����ѡ�õ������У���ˮ���ڵ⻯�ص�����ֽ���۵��ۡ��ܰơ���ʳ�ף�����Ϊ����ѡ�õ�������________(�����)��
��3��ij����Һ�У�����2%��5%��NaNO2��ֱ���ŷŻ������Ⱦ�������Լ���ʹNaNO2ת��Ϊ�����������Ⱦ��N2����________(����)��
A��NaCl B��NH4Cl C��HNO3 D��ŨH2SO4
��4������ɲ���ƽ���»�ѧ����ʽ��
��Al����NaNO3����NaOH===��NaAlO2����N2������ ��
����Ӧ������ת��5 mol e���������ɱ�״����N2�����Ϊ________L��
��5�����������õ������£� NH4+����������Ӧ��������NO3����������Ӧ�������仯ʾ��ͼ����:

�ٵ�һ����Ӧ�� ��Ӧ������ȡ������ȡ�����
��1mol NH4+(aq)ȫ��������NO3��(aq)���Ȼ�ѧ����ʽ�ǣ� ��
��14�֣���1�� NaNO2 ��2�֣�����2�� �ڡ��ݣ�2�֣� ����3�� B��2�֣���
��4��10Al��6NaNO3��4NaOH===10NaAlO2��3N2����2H2O ��2�֣���11.2L��2�֣���
��5���ٷ��� ���� NH4+(aq)+2O2(g)==NO3��(aq) + H2O(l) + 2 H+(aq) ��H����346 kJ/mol��2�֣�
��������
�����������1���ڷ�Ӧ2NaNO2��4HI===2NO����I2��2NaI��2H2O�У�NaNO2�е�NԪ�صĻ��ϼ۽��ͣ��õ����ӣ�����ԭ��������������2������NaNO2�ܹ������������½�I-����ΪI2��I2��������Һ��Ϊ��ɫ���⻯�ص�����ֽ��ʳ�ף�ѡ���Ǣڢݣ���3������2%��5%��NaNO2����Һֱ���ŷŻ������Ⱦ�����Լ���ʹNaNO2ת��Ϊ�����������Ⱦ��N2��������Ӧ���л�ԭ�ԣ������������NH4Cl��ѡ����B����4�����ݵ���ת����Ŀ��ȼ�ԭ���غ��֪ʶ�ɵã���ѧ����ʽ�ǣ�10Al��6NaNO3��4NaOH== 10NaAlO2��3N2����2H2O�����ݷ���ʽ��֪��ת��30mol�ĵ��ӣ������3mol�����壬��������Ӧ������ת��5 mol e���������ɱ�״����N2�����Ϊ[(3��5mol)��30]��22.4mol/L=11.2L����5�����ڵ�һ���ķ�Ӧ�����ڷ�Ӧ�������������������Է�Ӧ�Ƿ��ȷ�Ӧ���ڸ���ͼ���֪1mol NH4+(aq)ȫ��������NO3��(aq)���Ȼ�ѧ����ʽ��NH4+(aq)+2O2(g)==NO3��(aq) + H2O(l) + 2 H+(aq) ��H����346 kJ/mol��
���㣺����������ԭ��Ӧ�����ʵ����á����ʵļ����Լ���ѡ��ѧ����ʽ���Ȼ�ѧ����ʽ����д���й�������ԭ��Ӧ�ļ����֪ʶ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2015�����֣���и����ϵ�һ�Σ�10�£��¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
����˵������ȷ����( )
A�����³�ѹ�£�11.2 L���������е�ԭ����Ϊ6.02��1023
B�����³�ѹ�£�28 g���������е�ԭ����Ϊ6.02��1023
C��ͬ��ͬѹ�£���ͬ������κ����嵥��������ԭ����Ŀ��ͬ
D���ڱ�״���£�0.5��6.02��1023������������ռ�����Ϊ11.2 L
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�����ʡ�����и�����ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
�� NA Ϊ�����ӵ�����,����˵����ȷ����( )
A����״���£�0��1 mol Cl2 ����ˮ��ת�Ƶĵ�����ĿΪ0��1NA
B�����ʵ���Ũ��Ϊ0��1mol��L-1��MgCl2��Һ�У�����Cl������Ϊ0��2NA
C����״���£�2��24L�״��к���C��H������ĿΪ0��3NA
D�������£�22g CO2��N2O��������У����е�ԭ����ĿΪ1��5NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�����ʡ����9�µڶ��νο���ѧ�Ծ��������棩 ���ͣ�ѡ����
����˵����ȷ���� ( )
A����100 mL3 mol��L��1��H2 SO4��100 mL H2O��ϣ���������ʵ���Ũ�ȱ�Ϊ1.5 mol��L��1
B����100 g 20%��NaCl��Һ��100 g H2O��Ϻ�NaCl��Һ������������10%
C����200 mL 3 mol��L��1��BaCI2��Һ��I00 mL 3 mol��L��1��KCl��Һ��Ϻ���Һ�е�c��Cl-����Ȼ�� 3 mol��L��1
D����100 mL 20%��NaOH��Һ��100 mL H2O��Ϻ�NaOH��Һ������������10%
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�����ʡ����9�µڶ��νο���ѧ�Ծ��������棩 ���ͣ�ѡ����
NA���������ӵ�����������˵����ȷ���� ( )
A������NA����ԭ�ӵ������ڱ�״���µ����ԼΪ11.2L
B��2 L 1 mol��L��1�������������Ȼ��������ԼΪ2NA
C�����³�ѹ�£�ll.2L����������ԭ����ĿΪNA
D�������£�0.05 mol CO2��SO2���������������ԭ����Ϊ0.1NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ������ʡ������ѧ���������ۻ�ѧ�Ծ���A���������棩 ���ͣ�ѡ����
����ʵ�顰�����������롰���ۡ���Ӧ��ϵ��ȷ����
ѡ�� | ʵ����������� | ʵ����� |
A | �ò�˿��ij��Һ����ɫ��Ӧ������ʻ�ɫ | ����Һ��һ���������� |
B | ����������ͨ�뵽��ˮ�У���ˮ��ɫ | �����������Ư���� |
C | �ڵ��з�̪��Na2CO3��Һ�У��μ���BaC12��Һ����Һ��ɫ����ȥ�� | Na2CO3��Һ�д���ˮ��ƽ�� |
D | ij�����������ᣬ������ʹ����ʯ��ˮ����ǵ���ɫ��ζ���� | �ü�����K2CO3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�����ʡ��ˮ�и�����ѧ�ڵ��Ĵμ�⻯ѧ�Ծ��������棩 ���ͣ������
��16�֣�����п�̸ɵ�����й�������ȣ���������뻷�����������Σ����ij��ѧ��ȤС����������´����������շϵ���еĸ�����Դ��

��1���������60����ˮ�ܽ⣬Ŀ���� ��
��2������A������Ϊ ��
��3��ͭñ�ܽ�ʱ����H2O2��Ŀ���� ���û�ѧ����ʽ��ʾ����ͭñ�ܽ���ȫ�ɲ���_____________������ȥ��Һ�й�����H2O2��
��4������п�̸ɵ�صĵ����ΪKOH���ܷ�ӦΪZn+2MnO2+2H2O=2MnOOH+Zn(OH)2���为���ĵ缫��ӦʽΪ ��
��5����������Ҫ�ɷ�Ϊ���̻������̻�����м���һ������ϡ���ᡢϡ���ᣬ�����Ͻ�����������Ϊֹ����Ҫ��ӦΪ 2MnO(OH)+MnO2+2H2C2O4+3H2SO4=2MnSO4+4CO2��+6H2O��
�ٵ�1 mol MnO2�μӷ�Ӧʱ������ mol���ӷ���ת�ơ�
��MnO(OH)��Ũ�����ڼ���������Ҳ�ɷ�����Ӧ����д���÷�Ӧ�Ļ�ѧ����ʽ�� ��
��6��п�̸ɵ�������Ĺ�����KMnO4��Һ���ա��ڲ�ͬpH�£�KMnO4��Һ��Hg�������ʼ���Ҫ��������ͼ��ʾ��
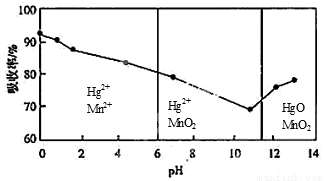
������ͼ��֪��
��pH��Hg�����ʵ�Ӱ���������pH���ߣ�����������__ _.
����ǿ���Ի�����Hg�������ʸߵ�ԭ�������KMnO4������������ ǿ.
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�����ʡ��ˮ�и�����ѧ�ڵ��Ĵμ�⻯ѧ�Ծ��������棩 ���ͣ�ѡ����
�����йؼ���ķ�������ȷ����
A���ڷ�Ӧ3Cu��8HNO3(ϡ)=2Cu(NO3)2��2NO����4H2O�У�����1molͭ������ʱ������ԭ������Ϊ2/3mol
B����amolFeS���뺬3amolH2SO4��Ũ�����У���ַ�Ӧ����������ԭ����ֱ���Fe3+��S��SO2����ų���SO2��������1.5a mol
C������ʱ�����ݻ�Ϊaml���Թ��г���NO2���壬Ȼ������ˮ�е�����ˮ�治������ʱΪֹ����ͨ��bmlO2�������Һ���ּ�������������Թ������ʣ������Ϊcml���Ҹ����岻��֧��ȼ�ա���a��b��c�Ĺ�ϵΪa=4b+3c
D��ij��Һ100ml�����к�����0.03mol������0.04mol�����ڸ���Һ��Ͷ��1.92 gͭ���ȣ���Ӧ��ų�һ����������ԼΪ0.015mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015����ʡӢ��ѧУ��һ��ѧ��12���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
����������ǿ������
A��1������ԭ��ʧȥ���ӵĶ���
B��1 mol�������ᷴӦ�ų������Ķ���
C��1 mol����ʧȥ���ӵĶ���
D������ԭ��ʧȥ���ӵ����׳̶�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com