
2013年初,全国各地多个城市都遭遇“十面霾伏”,造成“阴霾天”的主要根源之一是汽车尾气和燃煤尾气排放出来的固体小颗粒。
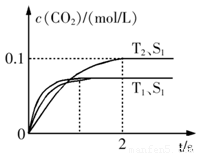
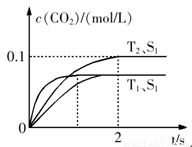
汽车尾气净化的主要原理为:2NO(g)+2CO(g)  2CO2+N2。在密闭容器中发生该反应时,c(CO2)随温度(T)、催化剂的表面积(S)和时间(t)的变化曲线如下图所示。据此判断:
2CO2+N2。在密闭容器中发生该反应时,c(CO2)随温度(T)、催化剂的表面积(S)和时间(t)的变化曲线如下图所示。据此判断:

(1)该反应为 反应(填“放热”或“吸热”):在T2温度下,0~2s内的平均反应速率:v(N2)= ;(2)当固体催化剂的质量一定时,增大其表面积可提高化学反应速率。若催化剂的表面积S1>S2,在答题卡上画出 c(CO2)在T1、S2条件下达到平衡过程中的变化曲线。
(3)某科研机构,在t1℃下,体积恒定的密闭容器中,用气体传感器测得了不同时间的NO和CO的浓度(具体数据见下表,CO2和N2的起始浓度为0)。
|
时间/s |
0 |
1 |
2 |
3 |
4 |
5 |
|
c(NO)/xl0-4 mol L-1 |
10.0 |
4.50 |
2.50 |
1.50 |
1.00 |
1.00 |
|
c(CO)/xl0-3 mol L-1 |
3.60 |
3.05 |
2.85 |
2.75 |
2.70 |
2.70 |
t1℃时该反应的平衡常数K= ,平衡时NO的体积分数为 。
(4)若该反应在绝热、恒容的密闭体系中进行,下列示意图正确且能说明反应在进行到t1时刻达到平衡状态的是 (填代号)。(下图中v正、K、n、m分别表示正反应速率、平衡常数、物质的量和质量)

(5)煤燃烧产生的烟气也含氮的氧化物,用CH4催化还原NOX可以消除氮氧化物的污染。
已知:CH4(g)+2NO2(g) = N2 (g)+CO2 (g)+2H2O(g) △H=-867.0 kJ • mol-1
2NO2 (g) 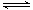 N2O4
(g)
△H=-56.9 kJ • mol-1
N2O4
(g)
△H=-56.9 kJ • mol-1
H2O(g) = H2O(l) △H=-44.0 kJ • mol-1
写出CH4催化还原N2O4 (g)生成N2 (g)、CO2 (g)和H2O(l)的热化学方程式 。
(1)放热 0.025 mol/(L·s) (各2分,共4分)
(2)见图(在T1S1下方,起点不变、终点在虚线后即可,合理均可)(2分)
(3)5000 L/mol (2分) 2.41% (2分)
(4)B D (共2分,少选得1分,错选不得分)
(5)CH4(g)+N2O4(g)═N2(g)+CO2(g)+2H2O(g) D H═ —898.1kJ/mol (2分)
【解析】
试题分析:⑴依据“先拐先平,数值大”的原则,可知:T1>T2,而在T1条件下可知,二氧化碳的含量反而低,可知,升高温度反应逆向移动,因此正向是放热的。化学反应速率等于单位时间内反应物或者生成物浓度的变化量,因此可以确定用二氧化碳表示的化学反应速率就为:0.050 mol/(L·s),再依据化学反应速率之比等于化学计量数之比,可知;用氮气表示的化学反应速率就为:0.025 mol/(L·s)。⑵增大表面积,只是增大反应速率,并不影响二氧化碳的含量,因此,只是反应达到平衡的时间延长,并不影响二氧化碳的量。
⑶
2NO(g)
+ 2CO(g)  2CO2 +
N2
2CO2 +
N2
起始浓度:10-3mol/L 3.6×10-3mol/L 0 0
转化浓度:9.0×10-4mol/L 9.0×10-4mol/L 9.0×10-4mol/L 4.5×10-4mol/L
平衡浓度:10-4mol/L 2.7×10-3mol/L 9.0×10-4mol/L 4.5×10-4mol/L
因此平衡常数: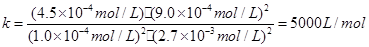
根椐,平衡时体积比等于物质的量之比,等于浓度之比,所以平衡时NO的体积分数为:


⑷A图中正反应速率反应开始后是减小的,错误;B图中表示的是化学平衡常数随时间的变化,因为是绝热的,而反应又是放热的,所以随着反应的进行,放出的热量散不出去,使反应逆向移动,使得平衡常数减小,但在某一个时刻达到平衡状态。正确;C图中在t1后各自的物质的量还在变化,则不是平衡状态,错误;D图中一氧化氮的质量在t1时刻质量不变,一定是一个平衡状态。正确。
⑸ ①CH4(g)+2NO2(g) = N2 (g)+CO2 (g)+2H2O(g) △H=-867.0 kJ • mol-1
②2NO2 (g) 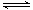 N2O4
(g)
△H=-56.9 kJ • mol-1
N2O4
(g)
△H=-56.9 kJ • mol-1
③H2O(g) = H2O(l) △H=-44.0 kJ • mol-1
①-②+③×2:CH4(g)+N2O4(g)═N2(g)+CO2(g)+2H2O(g) D H═ —898.1kJ/mol
考点:考查化学平衡,热化学的有关知识。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:2013-2014学年上海市十三校高三12月联考化学试卷(解析版) 题型:填空题
X、Y、Z、W是元素周期表前四周期常见的四种元素,原子序数依次增大。X原子核外有两种形状的电子云,四种伸展方向,常温下以双原子分子存在,性质稳定;Y的单质是生活中常见的合金材料成分之一,原子核外只有一个未成对电子,Z原子的半径比X大,其基态原子最外层的p电子是该层s电子的两倍,W是最常见的黑色金属之一。
(1)Z位于元素周期表中的位置是 ,W3+的最外层电子排布式是______,X的氧化物XO2与H2O比较,熔点较高的是______ (填化学式)。
(2)加热条件下,Z的单质与足量的X的最高价氧化物的水化物的浓溶液反应,生成 Z的最髙价含氧酸,写出此反应的化学方程式 。.
(3)比较Y、W性质的活泼性 (用一个化学反应方程式表示)。
(4)2013年初,全国各地多个城市都遭遇“十面霾伏”,造成“阴霾天”的主要根源之一是汽车尾气和燃煤尾气排放出来的固体小颗粒PM2.5。汽车尾气净化的主要原理为:2NO(g)+2CO(g)  2CO2(g)+N2(g)。在密闭容器中发生该反应时,c(CO2)随温度(T)、催化剂的表面积(S)和时间(t)的变化曲线如图所示。
2CO2(g)+N2(g)。在密闭容器中发生该反应时,c(CO2)随温度(T)、催化剂的表面积(S)和时间(t)的变化曲线如图所示。

据此判断:
该反应为 反应(放热、吸热);在T2温度下,0~2s内的平均反应速率:υ(N2)= ;
(5)当固体催化剂的质量一定时,增大其表面积可提高化学反应速率。若催化剂的表面积S1>S2,
在上图中画出c(CO2)在T1、S2条件下达到平衡过程中的变化曲线。
(6)若该反应在绝热、恒容的密闭体系中进行,下列示意图正确且能说明反应在进行到t1时刻达到平衡状态的是 (填代号)。
(下图中υ正、K、n、w分别表示正反应速率、平衡常数、物质的量和质量)

查看答案和解析>>
科目:高中化学 来源:2010年辽宁省高二6月月考化学试题 题型:选择题
2008年9月11日,全国各地多处发现婴儿因食用三鹿奶粉而出现肾结石的事件。当晚,三鹿集团承认婴幼儿奶粉受到三聚氰胺污染,并宣布召回市面上被污染的产品。三聚氰胺的分子结构如下:有关三聚氰胺的说法正确的是 ( )

A.三聚氰胺属于芳香族化合物,但不属于芳香烃;
B.三聚氰胺的分子式为C3N6H6;
C.三聚氰胺中的碳原子属于饱和碳原子;
D.三聚氰胺分子中的所有原子都在一个平面内
查看答案和解析>>
科目:高中化学 来源: 题型:
2008年9月11日,全国各地多处发现婴儿因食用三鹿奶粉而出现肾结石的事件。当晚,三鹿集团承认婴幼儿奶粉受到三聚氰胺污染,并宣布召回市面上被污染的产品。三聚氰胺的分子结构如下:有关三聚氰胺的说法正确的是 ( )
A.三聚氰胺属于芳香族化合物,但不属于芳香烃;
B.三聚氰胺的分子式为C3N6H6;
C.三聚氰胺中的碳原子属于饱和碳原子;
D.三聚氰胺分子中的所有原子都在一个平面内
查看答案和解析>>
科目:高中化学 来源:2010年辽宁省大连36中高二6月月考化学试题 题型:单选题
2008年9月11日,全国各地多处发现婴儿因食用三鹿奶粉而出现肾结石的事件。当晚,三鹿集团承认婴幼儿奶粉受到三聚氰胺污染,并宣布召回市面上被污染的产品。三聚氰胺的分子结构如下:有关三聚氰胺的说法正确的是 ( )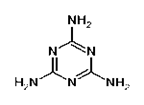
| A.三聚氰胺属于芳香族化合物,但不属于芳香烃; |
| B.三聚氰胺的分子式为C3N6H6; |
| C.三聚氰胺中的碳原子属于饱和碳原子; |
| D.三聚氰胺分子中的所有原子都在一个平面内 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com