
| 不稳定,自动失水 |

| 218-92 |
| 42 |
| 92-17×3+1 |
| 14 |





 高中必刷题系列答案
高中必刷题系列答案科目:高中化学 来源: 题型:
| 不稳定,自动失水 |



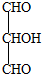
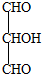




查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
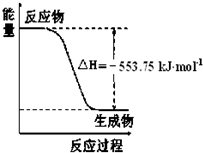 (1)盖斯定律认为:不管化学过程是一步完成或分数步完成,整个过程的总
(1)盖斯定律认为:不管化学过程是一步完成或分数步完成,整个过程的总查看答案和解析>>
科目:高中化学 来源: 题型:
(1)写出将绿色植物的秸秆转化为乙醇的化学方程式:________________________________。
(2)已知:C2H5OH(l)+3O2(g)![]() 2CO2(g)+3H2O(l);ΔH=-1 367 kJ·mol-1
2CO2(g)+3H2O(l);ΔH=-1 367 kJ·mol-1
CH4(g)+2O2(g)![]() CO2(g)+2H2O(l);ΔH=-890 kJ·mol-1
CO2(g)+2H2O(l);ΔH=-890 kJ·mol-1
若某种植物的秸秆含纤维素约50%,由植物秸秆经过一系列转化得到乙醇原料的总利用率为80%,则用1 000 g秸秆为原料制得的乙醇燃料燃烧所产生的热量与________L(标准状况下)甲烷完全燃烧产生的热量相当。
(3)绿色植物光合作用的效能是________________________________________________。
查看答案和解析>>
科目:高中化学 来源:2013届山西省忻州实验中学高三第一次模拟考试化学试卷(带解析) 题型:单选题
已知:C2H5OH(g)+3O2(g) ="==" 2CO2(g)+3H2O(g) ΔH1=-Q1kJ·mol-1;C2H5OH(g) ="==" C2H5OH(l) ΔH2=-Q2kJ·mol-1;H2O(g) ="==" H2O(l) ΔH3=-Q3kJ·mol-1;若使23g液体酒精完全燃烧,恢复到室温,则放出的热量为 ( )
| A.Q1+Q2+Q3 |
| B.0.5Q1-0.5Q2+1.5Q3 |
| C.0.5(Q1+Q2+Q3) |
| D.0.5Q1-1.5Q2+0.5Q3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com