
下列反应的离子方程式中,书写正确的是
A.碳酸氢钠溶液与氢氧化钠溶液反应:H++OH-=H2O
B.铝与烧碱溶液反应:Al+2H2O+OH-=AlO2-+ 2H2↑
C.碳酸钙溶于醋酸中:CaCO3+2H+=Ca2++H2O+CO2↑
D.向偏铝酸钠溶液中通入少量CO2:2AlO2-+CO2+3H2O=2Al(OH)3↓+ CO32-
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案科目:高中化学 来源:2017届辽宁省铁岭市协作体高三上联考四化学试卷(解析版) 题型:选择题
浓度均为0.10mol·L-1、体积均为V0的MOH与ROH溶液,分别加水稀释至体积V,pH随lg(V/ V0)的变化如图所示,下列叙述错误的是( )
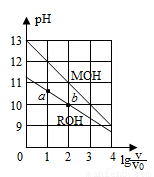
A.MOH的碱性强于ROH的碱性
B.ROH的电离程度:b点大于a点
C.若两溶液无限稀释,则它们的c(OH-)相等
D.当lg(V/ V0))=2时,若两溶液同时升高温度,则c(M+)/c(R+)增大
查看答案和解析>>
科目:高中化学 来源:2016-2017学年安徽省高一12月月考化学试卷(解析版) 题型:选择题
将一定量的Na2O2、Na2O、Na的混合物与足量的水反应,在标准状况下得到VL混合气体。将该混合气体通过电火花引燃,恰好完全反应,则原混合物中的Na2O2、Na2O、Na物质的量之比可能为( )
A.2:2:1 B.1:1:1 C.2 :l :2 D.l :l :2
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江苏省苏州市高二上学期学业模拟三化学试卷(解析版) 题型:填空题
⑴材料是人类赖以生存和发展的重要物质基础。
① 生产水泥的主要原料是黏土和 (填名称)。
② 橡胶是制造轮胎的重要原料,天然橡胶通过硫化措施可增大强度和弹性,硫化后的橡胶是 结构。(选填“线型”或“体型”)。
⑵人体健康与食品关系密切。
① 有些学生从小偏食,不爱吃水果、蔬菜,结果营养缺乏、发育不良,这主要是由于摄取 (选填“脂肪”、“维生素”或“蛋白质”)不足引起的。
② 生活中应合理地摄取人体必需的元素,体内 元素含量过低,会引起甲状腺疾病。
③ 糖类、油脂、蛋白质都是人体必需的营养物质。其中蛋白质被摄入人体后,在酶的作用下水解为________ (写名称)。
⑶人体健康与药物等关系密切:
①人的纯净胃液是一种无色液体,呈酸性,pH在0.9~1.5之间,其中H+的浓度比血液中高几万倍,回答下列问题:①胃液有帮助人体消化食物等多种功能,胃酸的主要成份是
②若胃酸酸度增大就会患胃酸过多症,下列物质不宜用做治疗胃酸过多的药物是
A、小苏打 B、氢氧化铝 C、氢氧化钠 D、碳酸镁
③胃舒平的主要成份是氢氧化铝,不溶于水且作用持久,写出该药物中和胃酸的离子方程式 。
④ 可以帮助流感病人解热镇痛的药物是 (选填“青霉素”或“阿司匹林”)。
⑷洁净安全的生存环境更是健康的保障。
①某农村地区洪涝灾害后为获得饮用水,在将地表水取回家后,先加明矾 , 再过滤,去除悬浮在水中的较大颗粒;过滤后常使用漂白粉进行杀菌消毒,其原理可用化学方程式表示为 。
②氯气与氢氧化钙溶液反应能制得漂白粉。试写出工业制漂白粉反应的化学方程式: 。
③通道口设有专门垃圾箱,箱体上标有右图所示,如图图标表示 。

查看答案和解析>>
科目:高中化学 来源:2016-2017学年江苏省苏州市高二上学期学业模拟三化学试卷(解析版) 题型:选择题
在如图所示的柠檬水果电池中,外电路上的电流从电极X流向电极Y。若X为铁,则Y可能是
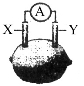
A.锌 B.石墨 C.银 D.铜
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江苏省苏州市高二上学期学业模拟三化学试卷(解析版) 题型:选择题
下列常见物质的俗名与化学式对应正确的是
A.烧碱—NaOH B.小苏打—Na2SO4
C.熟石灰—CaCl2 D.明矾—Al2(SO4)3
查看答案和解析>>
科目:高中化学 来源:2016-2017学年广西省钦州市钦州港区高一12月月考化学卷(解析版) 题型:计算题
已知常温下H2的密度是0.893gL-1。某烧杯中加入50.0mL水,并放入一小块金属钠,反应完全后冷却称量所得溶液,其质量为52.2g。试求:
(1)加入的钠的质量;
(2) 所得H2在常温下的体积;
所得H2在常温下的体积;
(3)所得溶液中NaOH的质量分数。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年广西省钦州市钦州港区高一12月月考化学卷(解析版) 题型:选择题
向含Na2CO3、NaAlO2的混合溶液中逐滴加入150mL1molL-1HCl溶液,测得溶液中的某几种离子物质的量的变化如图所示,则下列说法不正确的是
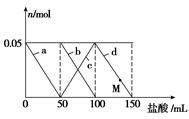
A.a曲线表示的离子方程式为: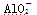 +H++H2O===Al(OH)3↓
+H++H2O===Al(OH)3↓
B.b和c曲线表示的离子反应是相同的
C.原混合溶液中的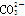 与
与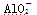 的物质的量之比为1∶2
的物质的量之比为1∶2
D.M点时,溶液中沉淀的质量为3.9g
查看答案和解析>>
科目:高中化学 来源:2017届四川省广元市高三上学期一诊化学试卷(解析版) 题型:填空题
氨是最重要的化工产品之一,其生产方法也在逐渐改进中,各国科学家均在为提高氨的产量,降低能耗做各种有益的探究; 氨在工业上有广泛用途。
(1)合成氨用的 H2 可以 CH4 为原料制得。已知相关的化学键键能数据如下:
则 CH4(g)与 H2O(g)反应生成 CO(g)和 H2(g)的热化学方程式 。
(2)近年有人将电磁场直接加在氮气与氢气反应的容器内,在较低的温度和压强条件下合成氨,获得了 较好的产率。从化学反应本质角度分析,电磁场对合成氨反应的作用是 。
(3)在 425℃、A12O3 作催化剂,甲醇与氨气反应可以制得(CH3)2NH。(CH3)2NH 显弱碱性,与盐酸反应 生成(CH3)2NH2Cl ,溶液中各离子浓度由小到大的顺序为 。
(4)直接供氨式碱性燃料电池的电池反应式 4NH3 + 3O2 = 2N2+ 6H2O,负极电极反应式为 。
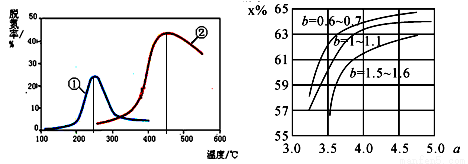
(5)如下图,采用 NH3 作还原剂,烟气以一定的流速通过两种不同催化剂,测量逸出气体中氮氧化物含 量,从而确定烟气脱氮率,反应原理为:NO(g) +NO2(g)+2NH3(g) 2N2(g) + 3H2O(g)。(注:脱氮率即氮氧化物转化率)
2N2(g) + 3H2O(g)。(注:脱氮率即氮氧化物转化率)
①对于气相反应,用某组分(B)的平衡压强(pB)代替物质的量浓度(cB)也 可以表示平衡常数(记作 KP),则上述反应的 KP=_______。
②以下说法正确的是________。
A.上述反应的正反应为吸热反应。
B.相同条件下,改变压强对脱氮率没有影响。
C.催化剂①、②分别适合于 250℃和 450℃左右脱氮
D.曲线①、②最高点表示此时平衡转化率最高
(6)氨气制取尿素[CO(NH2)2]的合成塔中发生反应:2NH3(g)+CO2(g) CO(NH2)2(l)+H2O(g)。下图 为合成塔中不同氨碳比 a [n(NH3)/n(CO2)] 和水碳比 b [n(H2O)/n(CO2)]时二氧化碳转化率(x%)。b 宜控制在__________(填序号)范围内
CO(NH2)2(l)+H2O(g)。下图 为合成塔中不同氨碳比 a [n(NH3)/n(CO2)] 和水碳比 b [n(H2O)/n(CO2)]时二氧化碳转化率(x%)。b 宜控制在__________(填序号)范围内
A.0.6~0.7 B.1~1.1 C.1.5~1.6
a 宜控制在 4.0 左右,理由是___________。
(7)氨氧化法制硝酸工业中,可用尿素溶液除去尾气中氮氧化物(NO 和 NO2)。尾气中的 NO、NO2 与 水反应生成亚硝酸,亚硝酸再与尿素反应生成对大气无污染的气体。1 mol 尿素能吸收工业尾气中氮氧化 物(假设 NO、NO2 体积比为 1:1)的质量为 g。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com