
����Ŀ����Ԫ�����������õ�������ѧ���ʣ����㷺Ӧ�������������С��Ӻ��ܷ���(��CoO��Co2O3������Al��Li��)����ȡ��CoCl2��6H2O������������ʾ��
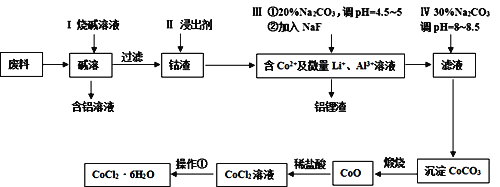
��ش��������⣺
(1)����I����Ҫ�����Ļ�ѧ��Ӧ����ʽΪ______��
(2)��֪Co2O3����ǿ�����ԣ�������II�н�����Ϊ���ᣬ��ɵĺ����_______��
(3)�������Тٵ�Ŀ���dz�ȥAl3+��д���ò���Ӧ�����ӷ���ʽ______��
(4)����ʵ��������CoCO3������Ĺ��������������ƾ��ƺͲ������⣬����______��______(����������)��
(5)����������HCl��Χ�н��еģ��䲽����______��_____�����ˡ�ϴ�ӡ����ϴ�ӹ����п����ù�ҵ�ƾ�����ˮ�����ŵ���_____��
(6)ijͬѧ�ñ���������Һ�ζ�δ֪Ũ�ȵ�CoCl2��Һ�����п���Ϊָʾ������____(��ѡ������������ӵ���ɫ����)
A��KCl B��KSCN C��K2CrO4 D��K2S
��֪����������20��ʱ����ɫ��Kspֵ���±�
��ѧʽ | AgCl | AgSCN | Ag2S | Ag2CrO4 |
��ɫ | ��ɫ | dz��ɫ | ��ɫ | ��ɫ |
Ksp | 2.0��10-10 | 1.0��10-12 | 2.0��10-48 | 2.0��10-12 |
���𰸡�2Al + 2NaOH +2H2O=2NaAlO2 + 3H2����2Li + 2H2O=2 Li OH + H2�� ������ж��������� 2Al3+ + 3CO32- + 3H2O=2Al(OH)3�� + 3CO2�� ���� ������ ����Ũ�� ��ȴ�ᾧ ���پ�����ܽ���ʧ C
��������
���ܷ���(��CoO��Co2O3������Al��Li)�����Һ��Al������ǿ����Һ����ƫ�����κ���������ܹ���ˮ�ܽ⣬���˵õ������ͺ�����Һ�������м���������õ�����Co2+����Li+��Al3+��Һ�������Һ�м���20%̼������Һ������Һ��pHΪ4.5-5֮�䣬Ȼ�����NaF�����˵õ����������Һ����Һ�м���30%̼������Һ������Һ��pHΪ8-8.5���õ�CoCO3����������̼���ܵõ�CoO��CoO�����ᷴӦ����CoCl2������Ũ������ȴ�ᾧ�����˷����CoCl2��6H2O�ᾧˮ����ݴ˷������
(1)����I��Al������ǿ����Һ����ƫ�����κ���������ܹ���ˮ�ܽ⣬��������Ҫ��ѧ��Ӧ����ʽ��2Al + 2NaOH +2H2O=2NaAlO2 + 3H2����2Li + 2H2O=2 Li OH + H2�����ʴ�Ϊ��2Al + 2NaOH +2H2O=2NaAlO2 + 3H2����2Li + 2H2O=2 Li OH + H2����
(2)Co2O3����ǿ�����ԣ�������II�н�����Ϊ���ᣬ�����е���Ԫ�ؿ��ܱ�����������������Ⱦ�������ʴ�Ϊ��������ж���������(��������������Ⱦ����)��
(3)�������Тٵ�Ŀ���dz�ȥAl3+��������̼�����ܹ�����˫ˮ�ⷴӦ����Ӧ�����ӷ���ʽΪ2Al3+ + 3CO32- + 3H2O=2Al(OH)3�� + 3CO2�����ʴ�Ϊ��2Al3+ + 3CO32- + 3H2O=2Al(OH)3�� + 3CO2����
(4)ʵ��������CoCO3��Ҫ�������н��У�����Ĺ��������������ƾ��ƺͲ������⣬���������������ǣ��ʴ�Ϊ�������������ǣ�
(5)CoCl2�ܹ�ˮ�⣬���ɵ��Ȼ������ӷ�����˲���������Ҫ��HCl��Χ�н��У���CoCl2��Һ�л��CoCl2��6H2O���壬��Ҫ��������Ũ������ȴ�ᾧ�����ˡ�ϴ�ӡ����ϴ�ӹ����п����ù�ҵ�ƾ�����ˮ�����پ�����ܽ���ʧ���Ҿƾ��������ӷ������ھ������ʴ�Ϊ������Ũ������ȴ�ᾧ�����پ�����ܽ���ʧ��
(6)ijͬѧ�ñ���������Һ�ζ�δ֪Ũ�ȵ�CoCl2��Һ�����ݼ���������20��ʱ����ɫ��Kspֵ���ζ���������Ҫ�����Ե�����Ӧ��ѡ��K2CrO4Ϊָʾ�����ʴ�Ϊ��C��


 Сѧ�̲�ȫ��ϵ�д�
Сѧ�̲�ȫ��ϵ�д� Сѧ��ѧ������ѿڶ���ϵ�д�
Сѧ��ѧ������ѿڶ���ϵ�д� ������Ӧ�������������ϵ�д�
������Ӧ�������������ϵ�д� �㽭֮�ǿ�ʱ�Ż���ҵϵ�д�
�㽭֮�ǿ�ʱ�Ż���ҵϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ж��л���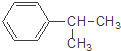 �������У�����ȷ���ǣ� ��
�������У�����ȷ���ǣ� ��
A. ��������ˮ���������ڱ�
B. �����ʺ�������ͬ���칹�壨������������������5��
C. ����ʹ���Ը��������Һ��ɫ
D. һ���������Ժ�Ũ���ᡢŨ����Ļ�����������Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ������Ũ������������̹�����ȷ�Ӧ���Ʊ�������MnO2+4HCl(Ũ)![]() MnCl2+Cl2��+2H2O����ij��ȤС����ȡ��������������������ʵ��װ����ͼ����ش��������⣺
MnCl2+Cl2��+2H2O����ij��ȤС����ȡ��������������������ʵ��װ����ͼ����ش��������⣺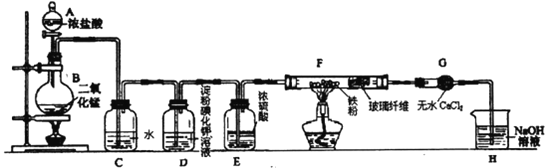
��1������A��������________��
��2�� C�з�Ӧ�Ļ�ѧ����ʽΪ____��������Һ��ˮ�����⣬�����еķ��Ӻ���������ȷ����____��
A��Cl2��HCl��HClO��H+��Cl�� B��Cl2��Mn2+��HClO��H+��Cl��
C��Cl2��HClO��H+��Cl����ClO�� D��Cl2��HCl��HClO��H+��Mn2+
��3��ʵ���й۲쵽D��Һ����ɫ�������ϵ�֪���۵⻯����Һ�ǵ��ۺ͵⻯�أ�KI���Ļ����Һ���ⵥ�ʣ�I2������������ɫ�����������Դ�KI���û����ⵥ�ʣ�д���÷�Ӧ�Ļ�ѧ����ʽΪ_________��
��4��F�����������۷�Ӧ�Ʊ���ˮ���Ȼ�����������֪�û�������غ�ɫ������ˮ���⣬100������ʱ������E��Ũ�����������___��˫ͨ��F�в�����ά�������뷴Ӧ����������________��
��5��H��ʢ��NaOH��Һ����������_____�� ������Ӧ�����ӷ���ʽΪ_____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������������У���ˮ �ڿ��� ���� �ܶ�����̼ ��H2SO4 ��NaOH��Һ �߰�ˮ ���Ȼ��� ������ ��NaHCO3
(1)���ڵ���ʵ���________________��
(2)���ڻ�������_________________��
(3)д����ˮ����Ҫ�ĵ��뷽��ʽ_______________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ���¶��£�����̼����MCO3(M��Mg2����Ca2����Mn��)�ij����ܽ�ƽ��������ͼ��ʾ������˵��������ǣ� ��
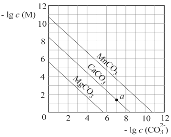
A. Ksp(MnCO3)��������Ϊ10��11
B. MgCO3������Һ�м�������ˮ�����c(Mg2��)����
C. ��Ũ�Ⱦ�Ϊ0.01mol��L��1��Mg2����Ca2����Mn2�������Һ����μ���Na2CO3��Һ�������γ�MgCO3����
D. a���ʾ����Һ�У�c(Ca2��)��c(CO32��)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����0.65gп�ӵ�50.0mLŨ��Ϊ1.00mol��L-1��������Һ�У��Լ��㣺��д��������̣�
(1)�ڱ�״���£����������������_________��
(2)����Ӧ��ɺ���Һ�����Ϊ50.0mL����ʱ��Һ�е�п����Ũ�Ⱥ�������Ũ�ȸ�Ϊ���٣�c(Zn2+)_________��c(H+)___________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʹ�õ�����CuSO45H2O������0.1 molL-1������ͭ��Һ����ȷ�IJ����ǣ�������
A. ���������ȳ�ȥ�ᾧˮ��ȡ16g�ܽ���1 Lˮ��
B. ��ȡ25 g��������ˮ��Ȼ����Һϡ����1 L
C. ��ȡ25 g�����ܽ���1 Lˮ��
D. ��16 g��������ˮ��Ȼ����Һϡ����1 L
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪һ����������������ȷֽ�Ļ�ѧ����ʽΪ��5NH4NO3![]() 2HNO3��4N2����9H2O������˵����ȷ����(����)
2HNO3��4N2����9H2O������˵����ȷ����(����)
A. �ֽⷴӦ����������ԭ��ӦB. N2�ǻ�ԭ���HNO3����������
C. �������뱻��ԭ�ĵ�ԭ����֮��Ϊ3��5D. ÿ����4mol N2ת��15mol����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���йؾ���Ľṹ����ͼ��ʾ������˵���в���ȷ���ǣ� ��
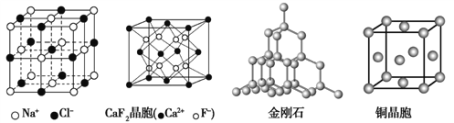
A. ��NaCl�����У���Na+�����Cl-�γ���������
B. ��CaF2�����У�ÿ������ƽ��ռ��4��Ca2+
C. �ڽ��ʯ�����У�̼ԭ������̼̼�������ı�Ϊ1:4
D. ͭ����Ϊ�����������ܶѻ����þ�������Խ��߳���Ϊԭ�Ӱ뾶��4��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com