
| A. | 属于同种元素 | B. | 属于同位素 | C. | 属于同种核素 | D. | 属于同种原子 |
分析 ${\;}_{86}^{222}$Rn、${\;}_{86}^{220}$Rn、${\;}_{86}^{219}$Rn的质子数都是86,属于同一种元素的三种不同核素(原子),互为同位素.
解答 解:A.${\;}_{86}^{222}$Rn、${\;}_{86}^{220}$Rn、${\;}_{86}^{219}$Rn的质子数都是86,属于同一种元素,故A正确;
B.${\;}_{86}^{222}$Rn、${\;}_{86}^{220}$Rn、${\;}_{86}^{219}$Rn是同一种元素的不同核素,互为同位素,故B正确;
C.${\;}_{86}^{222}$Rn、${\;}_{86}^{220}$Rn、${\;}_{86}^{219}$Rn所含有的中子数不同,不是同种核素,故C错误;
D.${\;}_{86}^{222}$Rn、${\;}_{86}^{220}$Rn、${\;}_{86}^{219}$Rn所含有的中子数不同,不是同种原子,故D错误;
故选AB.
点评 本题考查核素,难度不大,明确元素、同位素、核素的概念和关系是关键,注意基础概念的辨析.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
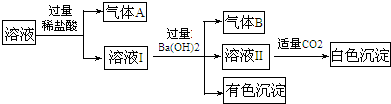
| A. | 气体B一定是NH3 | |
| B. | 白色沉淀一定是Al(OH)3 | |
| C. | 溶液中一定存在Al3+、Fe2+、NH4+、NO3- | |
| D. | 溶液中一定不存在大量的Na+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
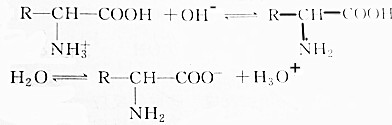
| A. | 增大溶液的pH,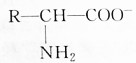 浓度减小 浓度减小 | |
| B. | 降低溶液的pH,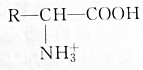 浓度减小 浓度减小 | |
| C. | 如溶液的pH适当,两种氨基酸离子的浓度可能相同 | |
| D. | pH改变,对电离方式无影响 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
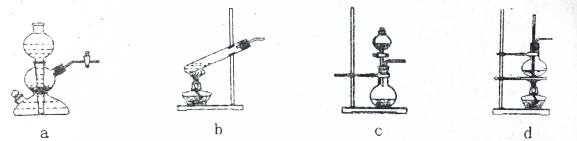
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 40.625 | B. | 42.15 | C. | 38.225 | D. | 42.625 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 滴定次数 | 待测液体积(mL) | 标准盐酸体积(mL) | |
| 滴定前读数(mL) | 滴定后读数(mL) | ||
| 第一次 | 10.00 | 0.50 | 20.40 |
| 第二次 | 10.00 | 4.00 | 24.10 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
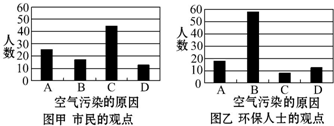
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com