
亚硝酰氯(ClNO)是有机合成中的重要试剂,工业上可用NO与Cl2合成,回答下列问题:
(1)一定条件下,氮氧化物与悬浮在大气中的海盐粒子相互作用时会生成亚硝酰氯,涉及热化学方程式和平衡常数如下表:
序号 | 热化学方程式 | 平衡常数 |
① | 2NO2(g)+NaCl(s) | K1 |
② | 4NO2(g)+2NaCl(s) | K2 |
③ | 2NO(g)+ Cl2(g) | K3 |
则ΔH3=_________(用ΔH1、ΔH2表示);K3=__________(用K1、K2 表示)
(2)300℃时,在一密闭容器中发生反应:2ClNO(g)  2NO(g)+ Cl2(g),其正反应速率表达式为v正=k·cn(ClNO)。测得速率和浓度的关系如下表:
2NO(g)+ Cl2(g),其正反应速率表达式为v正=k·cn(ClNO)。测得速率和浓度的关系如下表:
序号 | c(ClNO)/mol·L-1 | v正/mol·L-1·s-1 |
① | 0.30 | 3.60×10-9 |
② | 0.60 | 1.44×10-8 |
③ | 0.90 | 3.24×10-8 |
则n=________;k=___________;达到平衡后,若减小压强,则混合气体的平均分子量将_______(填“增大”、“减小”或“不变”)。
(3)25℃时,向体积为2L且带气压计的恒容密闭容器中通入0.08mol NO和0.04mol Cl2发生反应:2NO(g)+Cl2(g)  2ClNO(g) ΔH
2ClNO(g) ΔH
①若反应起始和平衡时温度相同,测得反应过程中压强(p)随时间(t)的变化如图Ⅰ曲线a所示,则ΔH________0(填“>”、“<”或“不确定”);若其他条件相同,仅改变某一条件时,测得其压强(p)随时间(t)的变化如图Ⅰ曲线b所示,则改变的条件是___________。
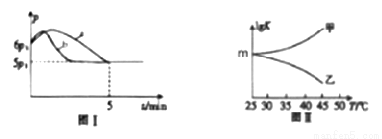
②图Ⅱ是甲、乙同学描绘上述反应平衡常数的对数值(lgK)与温度的变化关系,其中正确的曲线是____(填“甲”或“乙”);m值为_______________。
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2016-2017学年河北省唐山市高一3月月考化学试卷(解析版) 题型:选择题
短周期金属元素甲~戊在元素周期表中的相对位置如下表所示。下列判断正确的是:
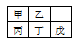
A. 原子半径: 丙<丁<戊 B. 氢氧化物碱性:丙>丁>戊
C. 金属性:甲>丙 D. 最外层电子数:甲>乙
查看答案和解析>>
科目:高中化学 来源:河北省唐山市2016-2017学年高二3月月考化学试卷 题型:推断题
某烃A的相对分子质量为84.回答下列问题:
(1)烃A的分子式为 。
(2)下列物质与A以任意比例混合,若总物质的量一定,充分燃烧消耗氧气的量不变的是 ;若总质量一定,充分燃烧消耗氧气的量不变的是 。
A. C7H8 B.C6H14 C.C7H14 D.C8H8
C7H8 B.C6H14 C.C7H14 D.C8H8
(3)若烃A为链烃,分子中所有的碳原子在同一平面上,该分子的一氯取代物只有一种。
① A的结构简式为 名称为 。
② 链烃A与Br2的CCl4溶液反应生成B,写出由A生成B的化学方程式: 。
③ 与A互为同分异构体,且主链碳原子个数与A相同的链烃有 种(不包括A)
(4)若A不能使溴水褪色,且其一氯代物只有一种,则A的结构简式为 。
查看答案和解析>>
科目:高中化学 来源:河北省唐山市2016-2017学年高二3月月考化学试卷 题型:选择题
下列各烃分别与H2完全加成,不能生成2,2,3—三甲基戊烷的是
A.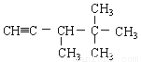
B.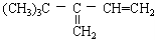
C.CH2=CHC(CH3)2CH(CH3)2
D.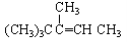
查看答案和解析>>
科目:高中化学 来源:河北省唐山市2016-2017学年高二3月月考化学试卷 题型:选择题
下列烯烃中存在顺反异构体的是( )
A.丙烯 B.1-丁烯
C.2-戊烯 D.2-甲基-2-丁烯
查看答案和解析>>
科目:高中化学 来源:2017届安徽省合肥市高三第二次教学质量检测理综化学试卷(解析版) 题型:选择题
W、X、Y、Z是原子序数依次最大的短周期元素,W的原子半径最小,W、Y同主族,X、Z同主族,且X、Z的原子序数之和是W、Y原子序数之和的2倍,下列说法中不正确的是
A. 由W和X两种元素形成的化合物可能含有非极性共价键
B. 由X、Y、Z三种元素形成的化合物只能为Y2ZX2或Y2ZX4
C. 由W、X、Y、Z四种元素形成的化合物水溶液可能呈强酸性
D. W、X、Y、Z四种元素两两之间形成二元化合物
查看答案和解析>>
科目:高中化学 来源:2017届福建省高三下学期模考4理科综合化学试卷(解析版) 题型:实验题
目前流行的关于生命起源假设的理论认为,生命起源于约40亿年前的古洋底的热液环境。这种环境系统中普遍存在铁硫簇结构,如Fe2S2、Fe4S4、Fe8S7等,这些铁硫簇结构参与了生命起源的相关反应。某化学兴趣小组在研究某铁硫簇结构的组成时,设计了下列实验。【实验Ⅰ】硫的质量确定
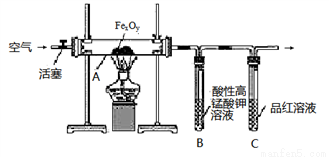
按图连接装置,检查好装置的气密性后,在硬质玻璃管A中放入1.00 g铁硫簇结构(含有部分不反应的杂质),在试管B中加入50.00 mL 0.1000 mol•L-1的酸性KMnO4溶液,在试管C中加入品红溶液。通入空气并加热,发现固体逐渐转变为红棕色。待固体完全转化后将B中溶液转移至250 mL容量瓶,洗涤试管B后定容。取25.00 mL该溶液用0.01000 mol•L-1的草酸(H2C2O4)进行测定剩余KMnO4溶液浓度的滴定。记录数据如下:
滴定次数 | 待测溶液体积/mL | 草酸溶液体积/mL | |
滴定前刻度 | 滴定后刻度 | ||
1 | 25.00 | 1.50 | 23.70 |
2 | 25.00 | 1.02 | 26.03 |
3 | 25.00 | 0.00 | 24.99 |
相关反应:① 2MnO4- + 2H2O + 5SO2 2Mn2+ + 5SO42- + 4H+
2Mn2+ + 5SO42- + 4H+
② 2MnO4- + 6H+ + 5H2C2O4 2Mn2+ +10CO2↑+ 8H2O
2Mn2+ +10CO2↑+ 8H2O
【实验Ⅱ】铁的质量确定
将实验Ⅰ硬质玻璃管A中的残留固体加入稀盐酸中,充分搅拌后过滤,在滤液中加入足量的NaOH溶液,过滤后取滤渣,经充分灼烧得0.600 g固体。
试回答下列问题:
(1)检查“实验Ⅰ”中装置气密性的方法是_______________。
(2)滴定终点的判断方法是______________。
(3)试管C中品红溶液的作用是_______________;有同学提出,撤去C装置,对实验没有影响,你的看法是___(选填“同意”或“不同意”),理由是________________。
(4)根据实验Ⅰ和实验Ⅱ中的数据可确定该铁硫簇结构的化学式为___________________。
【问题探究】
滴定过程中,细心的小明发现该KMnO4颜色褪去的速率较平常滴定时要快得多。为研究快的原因,甲同学继续进行了下列实验,实验数据如下表:
编号 | 温度/℃ | 酸化的H2C2O4溶液/mL | KMnO4溶液/mL | 溶液褪色时间/s |
1 | 25 | 5.0 | 2.0 | 40 |
2 | 25 | 5.0(另加少量可溶于水的MnSO4粉末) | 2.0 | 4 |
3 | 60 | 5.0 | 2.0 | 25 |
(5)分析上述数据,滴定过程中反应速率较快的原因可能是_____________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年北京市怀柔区高一上学期期末考试化学试卷(解析版) 题型:选择题
下列物质中既能与稀H2SO4反应, 又能与NaOH溶液反应的是
①NaHCO3 ②Al2O3 ③Al(OH)3 ④Al ⑤Na2CO3
A.③④ B.①②③④ C.②③④ D.全部
查看答案和解析>>
科目:高中化学 来源:北京市怀柔区2016-2017学年度第一学期期末考试高二化学试卷 题型:选择题
下列叙述不正确的是
A. 可用溴的四氯化碳溶液区分直馏汽油和裂化汽油
B. 蛋白质溶液中加入浓的硫酸铵溶液会有蛋白质析出
C. 甲烷、苯、乙醇、乙酸和酯类都可以发生取代反应
D. 相对分子质量相近的醇和烷烃,烷烃的沸点远远高于醇
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com