
一定条件下,24mL的CO2和N2的混合气体通过足量的过氧化钠粉末,充分反应后得到相同状况下的气体20ml,则原混合气体中CO2的体积分数为( )
A. 33.3% B. 44% C. 56% D. 66.7%
科目:高中化学 来源:2017届辽宁省庄河市高三上学期期末考试理综化学试卷(解析版) 题型:简答题
镁及其化合物有广泛用途.工业上以菱镁矿(主要成分为MgCO3,含SiO2以及少量FeCO3等杂质)为原料制备纳米氧化镁的实验流程如下
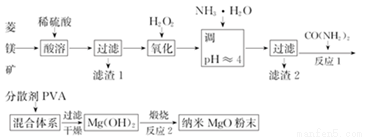
回答下列问题:
(1)滤渣1为____________(填化学式),CO(NH2)2的电子式为______。
(2)在实验室煅烧滤渣2制得的金属氧化物为______(填化学式),需要的仪器除酒精灯、三脚架以外,还需要______(填名称)。
(3)在一定条件下CO(NH2)2可与H2O反应生成CO2和一种弱碱,反应的化学方程式为__________。
(4)室温时,加入CO(NH2)2,产生沉淀。当 Mg2+沉淀完全时,溶液中的c(OH-)=_______(离子浓度小于1.0×10-5 mol•L-1时,即可认为该离子沉淀完全;室温时,Ksp[Mg(OH)2]=1.96×10-11)
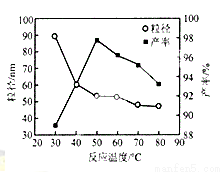
(5)工业上还可用氯化镁和碳酸铵为原料,采用直接沉淀法制务纳米MgO。如图为反应温度对纳米MgO产率和粒径的影响,据图分析反应的最佳温度为__________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江西省景德镇市高二(素质班)上学期期末考试化学试卷(解析版) 题型:推断题
石油的裂解是石油化工的重要方法之王,石油的裂解产物是合成材料的重要的基础原料。例如工业上以丙烯为原料可制得一种重要合成橡胶IR和一种合成树脂X。
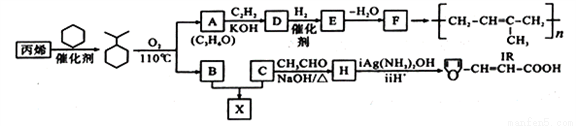
B的分子式是C6H6O,可与NaOH溶液反应。
已知以下信息:
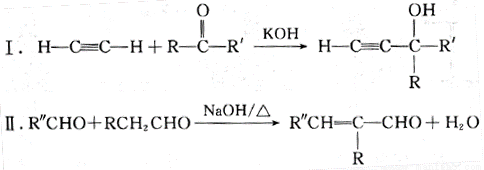
(—R、—R’、—R’’表示可能相同或可能不同的原子或原子团。)
Ⅲ.同一碳原子上有两个碳碳双键时,分子不稳定。
请回答下列问题。
在一定条件下,丙烯可与下列物质反应的是__________。
A、H2O B、NaOH溶液 C、Br2的CCl4溶液 D、酸性KMnO4溶液
(2)A与C2H2合成D的化学方程式是___________________,反应类型是______________。
(3)E、F中均含有碳碳双键,则E的结构简式是_____________。
(4)H的结构简式是_____________。
(5)B与C在一定条件下反应生成合成树脂X的化学方程式是_____________。
(6)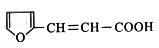 有多种同分异构体,符合下列要求的有___________种,其中在核磁共振氢谱中只出现四组峰的有_________种。
有多种同分异构体,符合下列要求的有___________种,其中在核磁共振氢谱中只出现四组峰的有_________种。
能与FeCl3溶液反应显紫色 ②只能发生银镜反应,不能发生水解反应
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江西省景德镇市高二(素质班)上学期期末考试化学试卷(解析版) 题型:选择题
下列实验能获得成功的是( )
选项 | 实验目的 | 实验步骤 |
A | 比较CH3COOH和H2CO3酸性强弱 | 测同浓度的Na2CO3、CH3COONa溶液的pH |
B | 比较S和Si非金属性强弱 | 向Na2SiO3溶液中通入SO2出现浑浊 |
C | 除去KNO3中少量NaCl | 将混合物制成热的饱和溶液,冷却结晶,过滤 |
D | 探究蔗糖水解的产物中是否含有葡萄糖 | 取少量蔗糖溶液加稀硫酸,水浴加热几分钟后,再加入新制的氢氧化铜悬浊液并且加热 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源:2016-2017学年辽宁省庄河市高一上学期期末考试化学试卷(解析版) 题型:简答题
铁、铝、硅及其化合物在生产、生活中有广泛的用途。试回答下列问题:
(1)常用作红色油漆和涂料的铁的氧化物是__________(写化学式)。将少量该氧化物溶于稀盐酸中,并滴加几滴KSCN溶液,再加入过量的铁粉,振荡,这时看到的现象是_______________。
(2)“铝粉”的俗称为“银粉”,皆因铝粉色泽如银。“银粉”质轻,遇明火即炸,写出反应的化学方程式 _____________________。“银粉”与烧碱溶液反应的离子方程式为______________________。
(3)硅的原子结构示意图为____________,水玻璃可用作木材防火剂,其主要成分是(写化学式)________。写出工业生产粗硅的化学方程式_______________________。高温条件下,二氧化硅、碳粉、氮气以物质的量之比3∶6∶2反应可以生成氮化硅陶瓷(一种新型无机非金属材料,具有耐高温、耐磨、抗氧化等特性)和另一种气体化合物,该反应的化学方程式为______________________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年辽宁省庄河市高一上学期期末考试化学试卷(解析版) 题型:选择题
烧杯中盛有含Mg2+、Al3+、Fe3+、Na+、Fe2+、Cl-六种离子的溶液,若向其中加入足量的Na2O2搅拌,充分反应后再向该烧杯中滴加足量的稀盐酸,此时上述离子物质的量保持不变的有( )
A. 1 种 B. 2 种 C. 3 种 D. 4种
查看答案和解析>>
科目:高中化学 来源:2016-2017学年辽宁省庄河市高一上学期期末考试化学试卷(解析版) 题型:选择题
将100gNa2CO3和NaHCO3的混合物用酒精灯加热至质量不再变化时,固体质量减少到75.2g。此混合物中Na2CO3的质量分数是( )
A. 75.2% B. 67.2% C. 41.7% D. 32.8%
查看答案和解析>>
科目:高中化学 来源:2017届山东省淄博市高三第一次模拟考试化学试卷(解析版) 题型:推断题
双安妥明可用于降低血液中的胆固醇,其结构简式为:

该物质的合成线路如下:
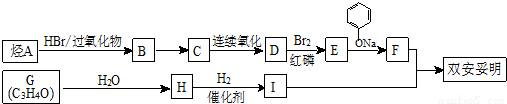
已知:I. 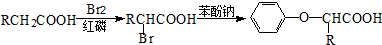
II. RCH═CH2 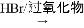 RCH2CH2Br
RCH2CH2Br
III.同温同压下A的密度是H2密度的28倍,且支链有一个甲基;G能发生银镜反应,且1molG能与2molH2发生加成反应。
(1)双安妥明的分子式为___________________。
(2)A的结构简式为___________________。
(3)反应B→C的反应条件是______________,G→H的反应类型是________________。
(4)反应“F+I→双安妥明”的化学方程式为___________________。
(5)符合下列3个条件的F的同分异构体有____________种。条件:①与FeCl3溶液显色;②苯环上只有两个取代基;③1mol该物质最多可与3molNaOH反应。
(6)参照上述合成路线,请设计由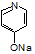 (
(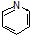 与苯环性质相似)与
与苯环性质相似)与 苯合成
苯合成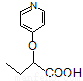 的路线______________。
的路线______________。
查看答案和解析>>
科目:高中化学 来源:2017届湖北省黄冈市高三第三次联考理综化学试卷(解析版) 题型:简答题
氮的氧化物种类较多,有N2O、NO、N2O3、NO2、N2O4、N2O5等,他们应用广泛。
(1)N2O是人类最早应用于医疗的麻醉剂之一。它可由NH4NO3在加热条件下分解产生,此反应的化学方程式为___________。已知N2O与CO2分子具有相似的结构,试画出N2O的结构式_______。
(2)N2O4可作火箭高能燃料N2H4的氧化剂。
已知:2NO2(g) N2O4(g) △H =-akJ·mol-1;N2H4(g)+O2(g)=N2(g)+2H2O(g) △H =-bkJ·mol-1;
N2O4(g) △H =-akJ·mol-1;N2H4(g)+O2(g)=N2(g)+2H2O(g) △H =-bkJ·mol-1;
N2(g)+2O2(g)=2NO2(g) △H =+ckJ·mol-1;(a、b、c均大于0)。
写出气态腁在气态四氧化二氮中燃烧生成氮气和气态水的热化学方程式___________。
(3)平衡常数K可用反应体系中气体物质分压表示,即K表达式中用平衡分压代替平衡浓度,分压=总压×物质的量分数(例如p(NO2)=p总×x(NO2))。写出反应2NO2(g) N2O4(g) △H =-akJ·mol-1平衡常数Kp表达式________(用p总、各气体物质的量分数x表示)。
N2O4(g) △H =-akJ·mol-1平衡常数Kp表达式________(用p总、各气体物质的量分数x表示)。
(4)新型绿色硝化剂N2O5可以N2O4为原料用电解法制备,实验装置如图所示。则电极B接直流电源的____极,电解池中生成N2O5的电极反应式为_____________。
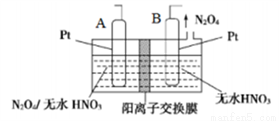
(5)可用氨水吸收NO2、O2生成硝酸铵,写出该反应的离子方程式_____________。
已知25℃时NH3·H2O的电离常数Kb=2×10-5,向500ml0.1mol·L-1硝酸铵溶液中通入标准状况下至少____ml氨气,使溶液呈中性(溶液的体积变化忽略不计)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com