
| A. | CO2 | B. | COCl2 | C. | C2H6O | D. | H2O2 |
分析 单键中含有一个σ键,双键中含有一个σ键和一个π键,三键中含有一个σ键和二个π键,据此分析.
解答 解:A.二氧化碳的结构式为O=C=O,所以含有双键,则一定既含σ键又含π键,故A正确;
B.COCl2的结构式为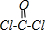 ,所以含有单键和双键,则一定既含σ键又含π键,故B正确;
,所以含有单键和双键,则一定既含σ键又含π键,故B正确;
C.C2H6O的结构中只有单键,没有双键,所以该分子中不含π键,故C错误;
D.H2O2的结构式为H-O-O-H,该分子中只含单键,所以该分子中不含π键,故D错误;
故选AB.
点评 本题考查分子中的化学键,明确分子结构即可解答,熟记常见分子结构,注意双氧水分子结构及其电子式,注意双氧水分子不是直线型结构,为易错点.


 金版课堂课时训练系列答案
金版课堂课时训练系列答案 单元全能练考卷系列答案
单元全能练考卷系列答案 新黄冈兵法密卷系列答案
新黄冈兵法密卷系列答案科目:高中化学 来源: 题型:选择题
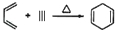 ,如果要合成
,如果要合成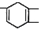 ,所用的起始原料可以是( )
,所用的起始原料可以是( )| A. | CH2=C(CH3)CH=CH2和CH≡C-CH2CH3 | B. | CH2=CHCH=CHCH3和CH3C≡CCH3 | ||
| C. | CH2=C(CH3)C(CH3)=CHCH3和CH≡CH | D. | CH2=C(CH3) C(CH3)=CH2和CH3C≡CH |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
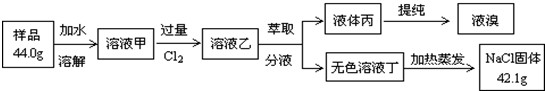
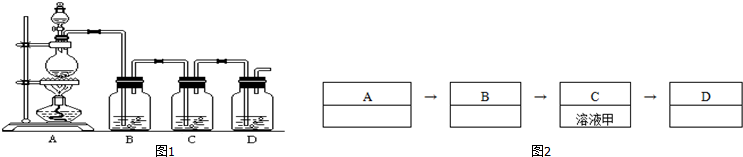
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H+、Na+、Cl-、ClO- | B. | K+、NO3-、Cl-、CO32- | ||
| C. | NH4+、Ca2+、OH-、HCO3- | D. | Al3+、NO3-、SO42-、MnO4- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
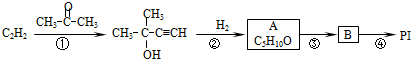
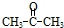 ”改为“乙醛”,经过②③④后得到产物的结构简式是
”改为“乙醛”,经过②③④后得到产物的结构简式是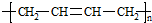 .
.

 +n NaOH→
+n NaOH→ +n CH3COONa.
+n CH3COONa.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com