
异戊二烯是重要的有机化工原料,其结构简式为CH2=C(CH3)CH=CH2。
完成下列填空:
(1)化合物X与异戊二烯具有相同的分子式,与Br/CCl4反应后得到3-甲基-1,1,2,2-四溴丁烷。X的结构简式为_______________。
(2)异戊二烯的一种制备方法如下图所示:

A能发生的反应有___________。(填反应类型)
B的结构简式为______________。
(3)设计一条由异戊二烯制得有机合成中间体 的合成路线。
的合成路线。
(合成路线常用的表示方式为: )
)
 发散思维新课堂系列答案
发散思维新课堂系列答案科目:高中化学 来源:2015-2016学年安徽省池州市高二5月考试化学试卷(解析版) 题型:简答题
有机物A分子中含苯环,相对分子质量136,分子中碳、氢原子个数相等,其含碳质量分数为70.6%,其余为氧、氢。
(1)A的分子式是__________________。
(2)若A分子中能发生银镜反应,且有弱酸性,则A的同分异构体有_______种,请任写一种符合条件的A的结构简式: 。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省邯郸市高一5月月考化学试卷(解析版) 题型:选择题
如图是电解硝酸银溶液的装置,其中c为银电极,d为铜电极,则下列有关判断正确的是( )

A.a为负极,b为正极
B.a为阳极,b为阴极
C.电解过程中,d电极质量减少
D.电解前后,电解池中银离子浓度保持不变
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广西南宁市高二下学期期中化学试卷(解析版) 题型:选择题
某溶液中由水电离出来的C(H+)=10-12mol/L,则该溶液中能大量共存的离子组是
A.K+、Na+、HCO3-、NO3-
B.Na+、SO42-、Cl-、S2-
C.NH4+、Mg2+、SO42-、NO3-
D. NO3-、K+、Na+、Cl-
查看答案和解析>>
科目:高中化学 来源:2016年全国普通高等学校招生统一考试化学(上海卷参考版) 题型:选择题
称取(NH4)2SO4和NH4HSO4混合物样品7.24 g,加入含0.1 mol NaOH的溶液,完全反应,生成NH3 1792 ml(标准状况),则(NH4)2SO4和NH4HSO4的物质的量比为
A.1:1 B.1:2 C.1.87:1 D.3.65:1
查看答案和解析>>
科目:高中化学 来源:2016年全国普通高等学校招生统一考试化学(上海卷参考版) 题型:选择题
下列气体的制备和性质实验中,由现象得出的结论错误的是
选项 | 试剂 | 试纸或试液 | 现象 | 结论 |
A | 浓氨水、生石灰 | 红色石蕊试纸 | 变蓝 | NH3为碱性气体 |
B | 浓盐酸、浓硫酸 | pH试纸 | 变红 | HCl为酸性气体 |
C | 浓盐酸、二氧化锰 | 淀粉碘化钾试液 | 变蓝 | Cl2具有氧化性 |
D | 亚硫酸钠、硫酸 | 品红试液 | 褪色 | SO2具有还原性 |
查看答案和解析>>
科目:高中化学 来源:2015-2016年浙江宁波效实中学高一下期中化学卷(选考)(解析版) 题型:推断题
下表为元素周期表的一部分,请参照元素①-⑧在表中的位置,用化学用语回答下列问题:
族
| IA | 0 | ||||||
1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
2 | ② | ③ | ④ | |||||
3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
(1)②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是______ ________;(用化学式表示)
(2)写出③形成的单质的结构式:_____ _______________;
写出②的最高价氧化物的电子式:_____ _______________;
写出⑧的最高价氧化物水化物的晶体类型:____ ______;
(3)写出工业制备⑦单质的化学方程式:____ ______;
(4)元素②和⑧的非金属性强弱,②的非金属性__ ______于⑧(填“强”或“弱”),并用化学方程式证明上述结论___________ ____________。
查看答案和解析>>
科目:高中化学 来源:2015-2016年浙江宁波效实中学高一下期中化学卷(创)(解析版) 题型:选择题
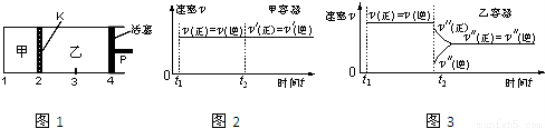
一定温度下可逆反应:A(s)+2B(g) 2C(g)+D(g);△H>0。现将1molA和2molB加入甲容器中,将4 molC和2 mol D加入乙容器中,此时控制活塞P,使乙的容积为甲的2倍,t1时两容器内均达到平衡状态(如图1所示,隔板K不能移动)。下列说法正确的是
2C(g)+D(g);△H>0。现将1molA和2molB加入甲容器中,将4 molC和2 mol D加入乙容器中,此时控制活塞P,使乙的容积为甲的2倍,t1时两容器内均达到平衡状态(如图1所示,隔板K不能移动)。下列说法正确的是
A.保持温度和活塞位置不变,在甲中再加入1 mol A和2 mol B,达到新的平衡后,甲中C的浓度是乙中C的浓度的2倍
B.保持活塞位置不变,升高温度,达到新的平衡后,甲、乙中B的体积分数均增加
C.保持温度不变,移动活塞P,使乙的容积和甲相等,达到新的平衡后,乙中C的体积分数是甲中C的体积分数的2倍
D.保持温度和乙中的压强不变,t2时分别向甲、乙中加入等质量的氦气后,甲、乙中反应速率变化情况分别如图2和图3所示(t1前的反应速率变化已省略)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com