
【题目】短周期元素A、B、C、D的原子序数依次增大。X、Y、Z、W分别是由这四种元素中的两种组成的常见化合物,Y为淡黄色固体,W为常见液体;甲为单质,乙为红棕色气体;上述物质之间的转化关系如图所示(部分生成物已省略)。则下列说法中不正确的是
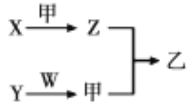
A. 沸点:W>X
B. 原子半径:D>B>C>A
C. C、D两种元素组成的化合物只含有离子键
D. A、B、C三种元素组成的化合物既可以是离子化合物,又可以是共价化合物
【答案】C
【解析】
乙为红棕色气体,乙是NO2 ;Y为淡黄色固体,Y是Na2O2;Y与W生成甲,所以甲是O2,W是常见液体则为H2O,甲与Z生成NO2,所以Z是NO ;X与O2生产NO2,所以X是NH3;因为A、B、C、D的原子序数依次增加,所以分别是H、N、O、Na;综上所述,A、B、C、D分别是H、N、O、Na;X是NH3,Y是Na2O2,Z是NO,W是H2O,甲是O2,乙是NO2。
A. 常温下,W为水液态,X为氨气气态,沸点:W>X,故A正确;
B. 电子层越多,原子半径越大,同周期从左向右原子半径减小,则原子半径:D>B>C>A,故B正确;
C. 氧化钠中只含有离子键,过氧化钠中既有离子键,又含有共价键,故C错误;
D. H、N、O三种元素可组成硝酸,为共价化合物,又可组成硝酸铵,为离子化合物,故D正确;
答案选C。


科目:高中化学 来源: 题型:
【题目】按要求回答下列问题:
(1)在标准状况下,V L H2 中含有 N 个氢分子,则阿伏加德罗常数为_____mol-1
(2)8.5 g氢氧根离子含有的电子数目为________。
(3)已知8 g A能与32 g B恰好完全反应,生成22 g C和一定量的D;现将16 g A与70 g B混合,充分反应后,生成2 mol D和一定量的C,则D的相对分子质量为_________。
(4)标准状况下,8.96L的CH4和CO的混合气体,该混合气体对氢气的相对密度是9.5,则混合气体平均摩尔质量为____________,混合气体中CH4与CO的体积比为____。
(5)若在标准状况下,将VLHCl气体溶于1L水中,所得溶液密度为d g/mL,则此溶液的物质的量浓度为________mol/L。(用带字母的表达式回答)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2019年是“国际化学元素周期表年”。下列有关说法不正确的是
A. 制冷剂氟里昂-12(CCl2F2)的研发利用,充分体现了元素周期表的指导作用
B. 通过测定物质中![]() 的含量可以推断文物的年代
的含量可以推断文物的年代
C. 门捷列夫预言的“类铝” 镓(Ga)元素的发现,证实了元素周期律的科学性
D. 过渡元素Ti、Mo、W等的单质有耐高温,耐腐蚀的特点,其合金可以制造火箭、导弹、宇宙飞船等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C三种物质随着X的变化,Y发生相应的变化,其变化关系如图所示。

(1)若X表示的是物质的量,则Y表示的不可能是_____(填序号,下同)
①物质的量 ②物质的体积 ③物质所含分子或原子的数目 ④物质的摩尔质量
(2)若A、B、C均为气体且压强恒定时,X表示的是温度,则Y表示的可能是______。
①气体的质量 ②气体的分子数 ③气体的体积 ④气体的摩尔质量
(3)若A、B、C均为气体,Y表示在相同条件下气体的体积,X表示的是气体的质量。
①相同条件下A、B、C三种气体的密度由大到小的顺序是_____(用字母A、B、C表示,下同)。
②A、B、C三种气体的摩尔质量由大到小的顺序是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液中可能含有OH-、CO32-、AlO2-、SiO32-、SO42-、Na+、Fe3+、Mg2+、Al3+等离子。当向该溶液中逐滴加入一定物质的量浓度的盐酸时,发现生成沉淀的物质的量随盐酸溶液的体积变化的图像如图所示,下列说法正确的是
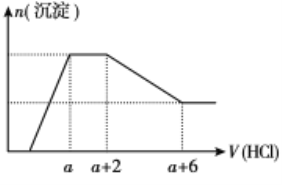
A. 原溶液中一定含有Na2SO4
B. 反应后最终溶液中的溶质只有AlCl3
C. 原溶液中含有CO32-与AlO2-的物质的量之比为1:1
D. 原溶液中一定含有的阴离子是OH-、SiO32-、AlO2-、CO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对下图的表达中正确的是( )

A.图a可以表示t s时,N2(g)+3H2(g) ![]() 2NH3(g)达到了平衡
2NH3(g)达到了平衡
B.图b中所介绍的电池使用后不能投入火中,应埋入地下以防污染环境
C.图c可表示某化学反应属于放热反应,放出的能量为E2-E1
D.图d涉及的反应可能为M![]() N
N
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】今年是门捷列夫发现元素周期律150周年。下表是元素周期表的一部分,W、X、Y、Z为短周期主族元素,W与X的最高化合价之和为8。下列说法错误的是

A. 原子半径:W<X
B. 常温常压下,Y单质为固态
C. 气态氢化物热稳定性:Z<W
D. X的最高价氧化物的水化物是强碱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关叙述正确的是( )
A.相同条件下,质量相等的CO和CO2它们所含的氧原子数目之比为11:7
B.同体积、同密度的C2H4和CO,两种气体的分子数一定相等
C.配制450mL0.1molL-1的NaOH溶液,用托盘天平称取NaOH固体1.8g
D.1L0.45molL-1NaCl溶液中Cl-的物质的量浓度比0.1L0.1 molL-1AlCl3溶液大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)某种原子的质量是a g,若NA只表示阿伏伽德罗常数的数值,该原子的相对原子质量为______,b g该原子的物质的量为______mol。
(2)a g A气体与b g B气体分子数相等,同温同压下,气体A与气体B的密度之比为___________。
(3)向10 mL 0.1mol/LNaHCO3溶液中缓缓滴入0.1mol/LCa(OH)2溶液,首先发生反应的两种离子为____________(填离子符号,下同),随后溶液中有白色沉淀生成,生成沉淀的两种离子为____________。当加入少量Ca(OH)2溶液时,发生的离子反应方程式为_______________________。
(4) 将3.22 g芒硝(Na2SO4·10H2O)溶于水中,要使每100个水分子中溶有1个Na+,则需加入水的质量为___g。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com