
下列说法正确的是 ( )
A 8g碳和14g氧气反应生成22g二氧化碳
B 二氧化碳由一个碳原子和两个氧原子构成
C 1g硫和1g氧气反应生成2g二氧化硫
D 水银温度计在温度升高时水银柱上升是因为汞原子的体积变大
 备战中考寒假系列答案
备战中考寒假系列答案科目:高中化学 来源: 题型:
二氧化氯(ClO2)是一种高效、广谱、安全的杀菌、消毒剂。
(1)氯化钠电解法是一种可靠的工业生产ClO2方法。
①用于电解的食盐水需先除去其中的Ca2+、Mg2+、SO 等杂质。其次除杂操作时,往粗盐水中先加入过量的________(填化学式),至沉淀不再产生后,再加入过量的Na2CO3和NaOH,充分反应后将沉淀一并滤去。经检测发现滤液中仍含有一定量的SO
等杂质。其次除杂操作时,往粗盐水中先加入过量的________(填化学式),至沉淀不再产生后,再加入过量的Na2CO3和NaOH,充分反应后将沉淀一并滤去。经检测发现滤液中仍含有一定量的SO ,其原因是___________【已知:Ksp(BaSO4)= 1.1 ×10-10 Ksp(BaCO3)= 5.1 ×10-9】
,其原因是___________【已知:Ksp(BaSO4)= 1.1 ×10-10 Ksp(BaCO3)= 5.1 ×10-9】
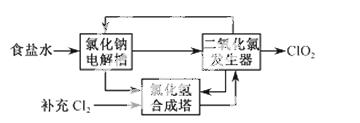
②该法工艺原理如右。其过程是将食盐水在特定条件下电解得到的氯酸钠(NaClO3)与盐酸反应生成ClO2。
工艺中可以利用的单质有____________(填化学式),发生器中生成ClO2的化学方程式为___________。
(2)纤维素还原法制ClO2是一种新方法,其原理是:纤维素水解得到的最终产物D与NaClO3反应生成ClO2。完成反应的化学方程式:
□ (D) +24NaClO3+12H2SO4=□ClO2↑+□CO2↑+18H2O+□_________
(3)ClO2和Cl2均能将电镀废水中的CN-氧化为无毒的物质,自身被还原为Cl-。处理含CN-相同量得电镀废水,所需Cl2的物质的量是ClO2的_______倍
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于混合物与纯净物的微观解释不正确的是( )
A、混合物是由多种微粒构成的
B、纯净物是由一种微粒构成的
C、混合物中各物质的微粒相互间不发生反应
D、混合物中各物质的微粒不再保持各自的化学性质
查看答案和解析>>
科目:高中化学 来源: 题型:
金秋十月,人们只要靠近盛开桂花的桂花树时,就能闻到怡人的桂花香。其原因是  ( )
( )
A.微粒体积很小 B.微粒之间有间隔C.微粒质量很小 D.微粒在不停的运动
查看答案和解析>>
科目:高中化学 来源: 题型:
已知元素M(只有一种化合价)的氧化物的化学式是M2O3,则它与硝酸根离子形成的化合物的化学式为  ( )
( )
A. M(NO3)2 B. M(NO3)3 C. MNO3 D. M2(NO3)2
查看答案和解析>>
科目:高中化学 来源: 题型:
从给定化合价的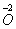 、
、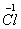 、
、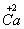 、
、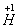 、
、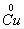 、
、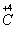 六种元素中,选择适当的元素,按下列要求组成物质(填写化学式)。
六种元素中,选择适当的元素,按下列要求组成物质(填写化学式)。
⑴单质 ___________ ; ⑵氧化物 _________ ;
⑶金属元素和非金属元素组成的化合物 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列化学方程式能正确表示所述内容的是
 A.铁丝在氧气中燃烧:4Fe+3O2 2Fe2O3
A.铁丝在氧气中燃烧:4Fe+3O2 2Fe2O3
B.常温下铝与氧气反应:2Al+O2=Al2O3
C.湿法炼铜:2Fe+3CuSO4=Fe2(SO4)3+3Cu
D.二氧化碳通入澄清石灰水:CO2 + Ca (OH)2 =CaCO3 ↓+ H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
已知Fe x O晶体的晶胞结构为NaCl型,由于晶体缺陷,x的值小于1。测知Fe x O晶体密度ρ为5.71g·cm–3,晶胞边长为4.28×10–10m(铁原子量为55.9,氧原子量为16.0)。求:
(1)FexO中x的值(精确至0.01)。
(2)晶体中的Fe分别为Fe2+ 和Fe3+,在Fe2+ 和Fe3+ 的总数中,Fe2+所占分数为多少?(精确至0.001。)
(3)写出此晶体的化学式。
(4)描述Fe在此晶体中占据空隙的几何形状(即与O2– 距离最近且等距离的铁离子围成的空间形状)。
(5)在晶体中,铁元素的离子间最短距离为多少?
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com