
 —、Cl—、NO3—中的一种或几种,取该溶液进行连续实验,实验过程如下:
—、Cl—、NO3—中的一种或几种,取该溶液进行连续实验,实验过程如下: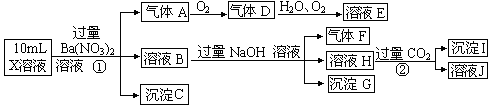
科目:高中化学 来源:不详 题型:填空题
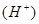 的能力由强到弱的顺序是 (用离子方程式加以说明)。
的能力由强到弱的顺序是 (用离子方程式加以说明)。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.含有18e-的两种氢化物中只存在极性键 |
| B.氢化物的沸点大小是H2O<H2S<H2Se<H2Te |
| C.a所对应的氢化物是H2O |
| D.每1mol H2S分解会吸收20KJ的热量 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 元素 | 相关信息 |
| X | X原子基态时最外层电子数是其内层电子数的2倍 |
| Y | Y原子基态时2p原子轨道上有3个未成对的电子 |
| Z | Z的基态原子最外层电子排布式为:nsnnpn+2 |
| W | W的原子序数为29 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.Y是第ⅦA族元素 | B.X是第二周期元素 |
| C.Y-与X2+的最外层电子数相同 | D.化合物XY2的化学键为离子键 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.Y、Z和W三种元素可能位于同一周期 |
| B.上述元素形成的氢化物中, W的氢化物相对分子质量最大,熔、沸点最高 |
| C.Y和W所形成的含氧酸均为强酸 |
| D.X、Y、Z和W可以组成原子的物质的量之比为5∶1∶4∶1的离子化合物 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.元素性质随原子序数的递增呈周期性变化的根本原因是元素的化合价呈周期性变化 |
| B.核外电子根据其能量的差别处于不同的电子层,能量越高离核越近 |
| C.所有原子的原子核都是由质子和中子构成的 |
| D.在元素周期表中具有相同的电子层数的主族元素,所处的周期序数相同 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

 。
。 )B的稀溶液与AgNO3溶液混合可形成沉淀AgX,此沉淀的Ksp(AgX) =1.8×10-10。将等体积的B稀溶液与AgNO3溶液混合,若B的浓度为2×10—4
)B的稀溶液与AgNO3溶液混合可形成沉淀AgX,此沉淀的Ksp(AgX) =1.8×10-10。将等体积的B稀溶液与AgNO3溶液混合,若B的浓度为2×10—4 mo1/L
mo1/L  ,则生成沉淀所需AgNO3溶液的最小浓度为________。若向AgX悬浊液中滴加KI溶液,观察到的现象 ,沉淀能够发生转化的原因是 。
,则生成沉淀所需AgNO3溶液的最小浓度为________。若向AgX悬浊液中滴加KI溶液,观察到的现象 ,沉淀能够发生转化的原因是 。查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com