
| A、通入硫化氢气体 |
| B、加入氯化钠溶液 |
| C、加入硫化钠溶液 |
| D、通入二氧化碳气体 |
科目:高中化学 来源: 题型:
| A、钠在氧气中燃烧发出白色光,生成淡黄色固体 |
| B、铁与稀硫酸反应,产生大量的气体,生成棕黄色溶液 |
| C、氢气在氯气中燃烧产生苍白色烟雾,生成有刺激性气味的气体 |
| D、铜与氯气反应产生棕黄色的烟,加水后溶液呈蓝绿色 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
 甲、乙、丙、丁均为中学化学中常见的单质或化合物,它们之间的转化关系如图所示(部分产物已略去),下列各组物质中不能按图示关系转化的是( )
甲、乙、丙、丁均为中学化学中常见的单质或化合物,它们之间的转化关系如图所示(部分产物已略去),下列各组物质中不能按图示关系转化的是( )| 选项 | 甲 | 乙 | 丙 | 丁 |
| A | NaOH | NaHSO3 | Na2SO3 | SO2 |
| B | AlCl3 | NaAlO2 | Al(OH)3 | NaOH |
| C | Fe | Fe(NO3)3 | Fe(NO3)2 | HNO3 |
| D | C | CO | CO2 | O2 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
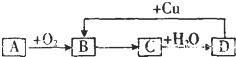 如图,A~D四种物质均含有同一种元素,A是非金属单质,D是最高价氧化物对应的水化物,则A、B、C、D中共同含有的元素可能是( )①C ②N ③Si ④S ⑤Cl.
如图,A~D四种物质均含有同一种元素,A是非金属单质,D是最高价氧化物对应的水化物,则A、B、C、D中共同含有的元素可能是( )①C ②N ③Si ④S ⑤Cl.| A、①② | B、②⑤ | C、③④ | D、②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| AB | CD | EF | |
| 离子电荷数 | 1 | 1 | 2 |
| 键长(10-10 m) | 2.31 | 3.18 | 2.10 |
| A、CD>AB>EF |
| B、AB>EF>CD |
| C、AB>CD>EF |
| D、EF>AB>CD |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、熔点:Li>Na>K>Rb |
| B、沸点:NH3<PH3<AsH3<SbH3 |
| C、热稳定性:CH4>PH3>H2O>HF |
| D、酸性:HClO>H2SO4>H3PO4>H2CO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com