
 ij����С��ͬѧ����ͼ��ʾװ�ý���C12���Ʊ����������ʵ�飨���ȼ��г�װ����ʡ�ԣ���
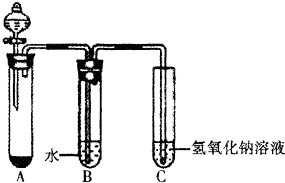
ij����С��ͬѧ����ͼ��ʾװ�ý���C12���Ʊ����������ʵ�飨���ȼ��г�װ����ʡ�ԣ������� ��1����A�й���ΪMnO2������Ũ���ᣬ��װ��ͼ��Aװ������������װ�ã����ö������̺�Ũ������ȷ�Ӧ�����Ȼ��̡�������ˮ���ݴ���д��ƽ��ѧ����ʽ��
��2��װ��B��Ϊ��ˮ��������ɫʯ����ֽ�ϣ�Ϊ������ˮ��Ӧ���ɵ������������ʱʯ����Һ���ɫ�����ɵĴ��������Ư���ԣ�ʹ��ɫ��ȥ��
��3��C��Ϊ�������ƣ�C12���������Ʒ�Ӧ�����Ȼ��ơ��������ƺ�ˮ��
��4������������ʵ���Ũ��C=$\frac{1{0}^{3}�Ѧ�}{M}$��
�ڷ�Ӧ�и������Ϊ��������Ũ����Ϊ��ԭ��������MnԪ�صĻ��ϼ�+7��+2����ClԪ�صĻ��ϼ�-1��0��������ӵ�ת�Ʒ������Ŀ��
��5����������Ԫ�صĻ��ϼۼ����������������ϼ۵Ĵ�����Ϊ0�����
�ڽ��������ԭ��Ӧ�л��ϼ�������ȣ��ж�ClO2��ClԪ�ػ��ϼ۱仯��Ԫ�ػ��ϼ����߱��ֻ�ԭ�ԣ�Ԫ�ػ��ϼ۽��ͱ��������ԣ�
�۽�Cl2ͨ������й���NaClO2�ķ�Ӧ���ڶ��߷�Ӧ���Ƶ�ClO2��NaClO2��Cl��+3�����ߵ�+4�ۣ�Cl2��ClԪ�صĻ��ϼ۴�0�۽��͵�-1�ۣ��䷴ӦΪ2NaClO2+Cl2�T2ClO2+2NaCl����Ϸ�Ӧ��֮��Ĺ�ϵ���㣮
��� �⣺��1����A�й���ΪMnO2������Ũ���ᣬ��Aװ������������װ�ã��������̺�Ũ������ȷ�Ӧ�����Ȼ��̡�������ˮ����Ӧ�Ļ�ѧ����ʽΪ��MnO2+4HCl��Ũ��$\frac{\underline{\;\;��\;\;}}{\;}$MnCl2+Cl2��+2H2O��
�ʴ�Ϊ��MnO2+4HCl��Ũ��$\frac{\underline{\;\;��\;\;}}{\;}$MnCl2+Cl2��+2H2O��
��2��װ��B��Ϊ��ˮ��������ɫʯ����ֽ�ϣ���Һ����ɫ���������ɫ��Ϊ��ɫ���ٱ�Ϊ��ɫ������Ϊ������ˮ��Ӧ��������ʹ����ᣬCl2+H2O=HCl+HClO������ʹǿ����ʹʯ����Һ��죬���ɵ�HClO����Ư����ʹʯ����ɫ��
�ʴ�Ϊ��Ư���ԣ�
��3��C��Ϊ�������ƣ�C12���������Ʒ�Ӧ�����Ȼ��ơ��������ƺ�ˮ����ӦΪ��C12+2NaOH=NaCl+NaClO+H2O��
�ʴ�Ϊ��C12+2NaOH=NaCl+NaClO+H2O��
��4������������ʵ���Ũ��C$\frac{1{0}^{3}�Ѧ�}{M}$=$\frac{1{0}^{3}��1.2��36.5%}{36.5}$mol/L=12mol/L��
�ʴ�Ϊ��12mol/L��
�ڷ�Ӧ�и������Ϊ��������Ũ����Ϊ��ԭ����MnԪ�صĻ��ϼ�+7��+2����ClԪ�صĻ��ϼ�-1��0����Ӧ���������ͻ�ԭ����ʧ������Ŀ��ȣ�
�ʴ�Ϊ�� ��
��
��5���ٶ������ȵĻ�ѧʽΪC1O2����Ԫ�صĻ��ϼ�Ϊ-2�ۣ���û���������Ԫ�صĻ��ϼ�Ϊx����x+��-2����2=0�����x=+4��
�ʴ�Ϊ��+4�ۣ�
�ڷ�Ӧ��FeԪ�ء�MnԪ�ػ��ϼ����ߣ����ݻ��ϼ�������ȣ�ClO2��ClԪ�ػ��ϼ۽��ͣ����������ԣ�
�ʴ�Ϊ��������
�۽�Cl2ͨ������й���NaClO2�ķ�Ӧ���ڶ��߷�Ӧ���Ƶ�ClO2��NaClO2��Cl��+3�����ߵ�+4�ۣ�Cl2��ClԪ�صĻ��ϼ۴�0�۽��͵�-1�ۣ��䷴ӦΪ2NaClO2+Cl2�T2ClO2+2NaCl����ԭ����ΪNaCl�������ı�״����11.2L Cl2����0.5mol������ClO2Ϊ1mol��������Ϊ1mol��67.5g/mol=67.5g��
�ʴ�Ϊ��NaCl��67.5��
���� ���⿼��������ʵ�鷽����ơ�������ԭ��Ӧ�ļ��㣬���ؿ������������������ԭ��Ӧ�е�ʧ������ȣ��������ʵ����ʽ��������ԭ��Ӧ�����������Ŀ�Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ȡ10.6 g��ˮ̼���ƣ�����100 mL����ƿ�У���ˮ�ܽ⡢���� | |
| B�� | ���ݺ�����ƿ����������ת��ҡ�� | |
| C�� | ת��Na2CO3��Һʱ��δ�ò�����������ֱ�ӵ�������ƿ�� | |
| D�� | ��ȡ10.6 g��ˮ̼���ƣ�����100 mL����ˮ�����衢�ܽ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | ����ƿϴ����δ���� | |
| B�� | ��Һ���ձ�δϴ�� | |
| C�� | ����ʱ���Ӷ��� | |
| D�� | ҡ�Ⱥ�Һ����ڿ̶����ٵμ�ˮ���̶��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 2�� | B�� | 3�� | C�� | 4�� | D�� | 5�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 �����ٴ���һ�ֽ�֬��Ѫ˨ҩ�����һ���ϳ�·����ͼ��
�����ٴ���һ�ֽ�֬��Ѫ˨ҩ�����һ���ϳ�·����ͼ��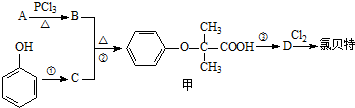
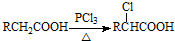
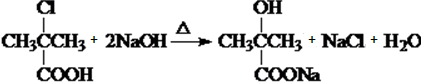 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ��ѧ��ʵ | ���ƽ��� | |
| A | �����£�pH=3������ϡ��1000����pH=6 | �����£�pH=6������ϡ��1 000����pH=9 |
| B | �������MgCl2����ȡ����þ | �������AlCl3Ҳ����ȡ������ |
| C | Na�Ż����øɱ���� | K�Ż�Ҳ�����øɱ���� |
| D | ��SO2ͨ��BaCl2��Һ���������� | ��SO2ͨ��Ba��NO3��2��Һ��Ҳ�������� |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ���� | ���� | ���۽��� | |
| A | �������ۼ�ϡ�����ַ�Ӧ������KSCN��Һ | ������ɫ��Һ | ϡHNO3����������Fe3+ |
| B | ijʵ��С��������ϻ����Ϣ��Fe3+�������������ʣ����������ַ�����ϴһ������������Ӧ���Թܣ�������Fe3+Ũ����ͬ��FeCl3��Һ��Fe2��SO4��3��Һ���ֱ�������ϴʵ�飮 | ��FeCl3��Һ��ϴ��Fe2��SO4��3��Һ��ϴ�øɾ� | ������ΪFe3+���������ʵĹ��̿�����һ��������̣�Fe3++Ag?Fe2++Ag+ |
| C | ��������Һ��ͨ������CO2���� | ��Һ����� | ̼������ǿ�ڱ��ӣ���Һ�л���Na2CO3���� |
| D | ���̼������Һͨ����CO2���� | �������� | ��Ϊ����Na2CO3 |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com