
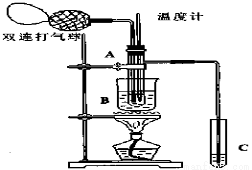
乙醛在氧化铜催化剂存在的条件下,可以被空气氧化成乙酸。依据此原理设计实验制得并在试管C中收集到少量乙酸溶液(如图所示:试管A中装有40%的乙醛水溶液、氧化铜粉末;试管C中装有适量蒸馏水;烧杯B中装有某液体)。已知在60℃~80℃时用双连打气球鼓入空气即可发生乙醛的氧化反应,连续鼓入十几次反应基本完全。有关物质的沸点见下表:

请回答下列问题:
(1)试管A内在60℃~80℃时发生的主要反应的化学方程式为 (注明反应条件)。
(2)如图所示在实验的不同阶段,需要调整温度计在试管A内的位置,在实验开始时温度计水银球的位置应在_____________,目的是 ;当试管A内的主要反应完成后温度计水银球的位置应在___________________,目的是____________________。
(3)烧杯B的作用是___________________________,烧杯B内盛装的液体可以是____________(写出一种即可,在题给物质中找)。
(4)若想检验试管C中是否含有产物乙酸,请你在所提供的药品中进行选择,设计一个简便的实验方案。所提供的药品有:pH试纸、红色的石蕊试纸、白色的醋酸铅试纸、碳酸氢钠粉末。实验仪器任选。该方案为 。
 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案 期末集结号系列答案
期末集结号系列答案科目:高中化学 来源:2016届河北省衡水市高三下仿真二理综化学试卷(解析版) 题型:选择题
X、Y、Z、M、 W为原子序数依次增大的5种短周期元素。X的质子总数与电子层数相同,Y、Z、M同周期且相邻,W原子核外电子数是M原子最外层电子数的2倍。Z与其同主族的短周期元素可形成常见的大气污染气体甲。X, Y, Z三种元素形成化合物乙。下列说法错误的是
A.气体甲可与Z的某种氢化物反应生成强酸
B.W元素的晶体单质是一种良好的半导体材料
C.化合物乙中一定只有共价键
D.X分别与Y、 Z、M、 W形成的常见化合物中,稳定性最好的是XM
查看答案和解析>>
科目:高中化学 来源:2015-2016学年陕西西安长安一中高二下第二次月考化学卷(解析版) 题型:选择题
有人设想合成具有以下结构的四种烃分子,下列有关说法不正确的是( )
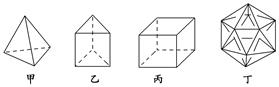
A.1 mol甲分子内含有10 mol共价 键
键
B.由乙分子构成的物质不能发生氧化反应
C.丙分子的二氯取代产物只有三种
D.分子丁是不可能合成的
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江西省高一下第三次考试化学试卷(解析版) 题型:选择题
有机物的种类繁多,但其命名是有规则的。下列有机物命 名正确的是
名正确的是
A. 1,4-二甲基丁烷
1,4-二甲基丁烷
B. 3-甲基丁烯
3-甲基丁烯
C. 2-甲基丁烷
2-甲基丁烷
D.CH2Cl-CH2Cl 二氯乙烷
查看答案和解析>>
科目:高中化学 来源:2016届海南省高三全真模拟二化学试卷(解析版) 题型:填空题
Ⅰ.化学与科学、技术、社会、环境密切相关,下列做法中正确的是__________。
A.研制乙醇汽油(汽油中添加一定比例乙醇)技术,不能降低机动车尾气中有害气体排放
B.工业上用石灰乳对煤燃烧后形成的烟气进行脱硫,最终能制得石膏
C.为了有效的发展清洁能源,采用电解水的方法大量制备H2
D.世博停车场安装催化光解设施,可将汽车尾气中CO和NOx反应生成无毒气体
II.浩瀚的海洋是一个巨大的资源宝库,蕴藏着丰饶的矿产,是宝贵的化学资源,下图是海水加工的示意图,根据下图回答问题。
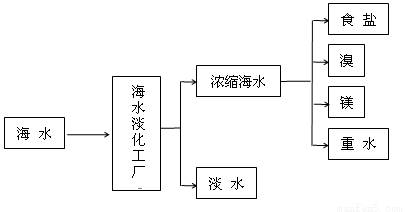
(1)海水淡化工厂通常采用的制备淡水的方法有 (写出两种)。
(2)下图是从浓缩海水中提取溴的流程图。写出下图中①②的化学式:① ,② ,吸收塔中发生的化学反应方程式为 。

(3)制备金属镁是通过电解熔融的MgC12,而不用MgO,其原因是 。
(4)食盐也是一种重要的化工原料,氯碱工业就是通过电解饱和食盐水来制备NaOH、H2和C12。海水中得到的粗盐中往往含有一些杂质,必须加入一些化学试剂,使杂质沉淀,处理后的盐水还需进入阳离子交换塔,其原因是 。电解食盐水在离子交换膜电解槽中进行,离子交换膜的作用是 。
(5)多晶硅主要采用SiHCl3还原工艺生产,其副产物SiCl4可转化为SiHCl3而循环使用。一定条件下,在20L恒容密闭容器中的反应:3SiCl4(g)+2H2(g)+Si(g) 4SiHCl3(g)。达平衡后,H2与SiHCl3物质的量浓度分别为0.140mol/L和0.020mol/L。若H2全部来源于氯碱工业,理论上需消耗纯NaCl的质量为 kg。
4SiHCl3(g)。达平衡后,H2与SiHCl3物质的量浓度分别为0.140mol/L和0.020mol/L。若H2全部来源于氯碱工业,理论上需消耗纯NaCl的质量为 kg。
查看答案和解析>>
科目:高中化学 来源:2016届海南省高三全真模拟二化学试卷(解析版) 题型:选择题
X、Y、Z、W是原子序数依次增大的四种短周期元素,甲、乙、丙、丁、戊是由其中的两种或三种元素组成的化合物,己是由Z元素形成的单质。已知:甲 + 乙 = 丁 + 己,甲 + 丙 = 戊 + 己; 0.1 mol·L-1丁溶液的pH为13(25℃)。下列说法正确的是
A.原子半径:W>Z>Y>X
B.Y元素在周期表中的位置为第三周期第ⅣA族
C.1mol甲与足量的乙完全反应共转移了1 mol电子
D.1.0 L 0.1 mol·L-1戊溶液中阴离子总的物质的量小于0.1 mol
查看答案和解析>>
科目:高中化学 来源:2016届海南省高三全真模拟二化学试卷(解析版) 题型:选择题
用NA表示阿伏加德罗常数的值。下列叙述正确的是
A.1.8 g重水(D2O)中含NA个中子
B.标准状况下,2.24 L Cl2与过量稀NaOH溶液反应,转移的电子总数为0.2 NA
C.室温下,21.0 g乙烯和丁烯的混合气体中含有的碳原子数目为1.5 NA
D.足量的铜与含2 mol H2SO4的浓硫酸充分反应,可生成NA个SO2分子
查看答案和解析>>
科目:高中化学 来源:2016届广西柳州铁路一中高三5月月考理科化学试卷(解析版) 题型:简答题
I.2015年国产C919大型客机正式下线,标志着我国成为世界上少数几个具有自行研制大型飞机的国家之一,标志着我国航空工业进入了新的发展阶段。
(1)飞机的外壳通常采用镁-铝合金材料,铝的价电子排布图为_______,第一电离能:镁___(填“大于”或“小于”)铝。
(2)现代飞机为了减轻质量而不减轻外壳承压能力,通常采用复合材料--玻璃纤维增强塑料,其成分之一为环氧树脂,常见的E51 型环氧树脂中部分结构如下图所示:其中碳原子的杂化方式为________,对应个数比为_________

II.大型飞机的发动机被誉为航空工业皇冠上的“宝石”。制造过程中通常采用碳化钨做关键部位的材料
(3)钨元素位于周期表的第六周期第VIB族,请写出其外围电子排布式___________
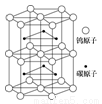
(4)下图为碳化钨晶体的一部分结构,碳原子嵌入金属钨的晶格的间隙,并不破坏原有金属的晶格,形成填隙+固溶体,也称为填隙化合物。在此结构中,其中钨原子有_______个,1个钨原子周围距离钨原子最近 的碳原子有______个,下列金属元素的堆积方式与碳化钨晶胞中碳原子和钨原子所处位置类似的是______
的碳原子有______个,下列金属元素的堆积方式与碳化钨晶胞中碳原子和钨原子所处位置类似的是______
A. Fe Cu B.Ti Au
C.Mg Zn D.Cu Ag
(5)假设该部分晶体的体积为Vcm3,碳化钨的摩尔质量为M g/mol,密度为b g/cm3,则阿伏加德罗常数NA用上述数据可以表示为___________________
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北武邑中学高一下第二次月考化学试卷(解析版) 题型:选择题
下列各物质的名称正确的是
A.3,3-二甲基丁烷
B.2,3,3-三甲基丁烯
C.2,2-二甲基-3-乙基丁烷
D.2,3-二甲基-4-乙基己烷
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com