
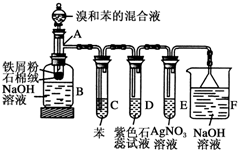
 苯和溴取代反应的实验装置如图所示,其中A为由具支试管改制成的反应容器,在其下端开了一小孔,塞好石棉绒,再加入少量铁屑粉.填写下列空白:
苯和溴取代反应的实验装置如图所示,其中A为由具支试管改制成的反应容器,在其下端开了一小孔,塞好石棉绒,再加入少量铁屑粉.填写下列空白: ,故答案为:
,故答案为: ;
;

 导学教程高中新课标系列答案
导学教程高中新课标系列答案 小学课时特训系列答案
小学课时特训系列答案科目:高中化学 来源: 题型:
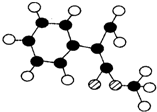 肉桂酸甲酯M,常用作调制具有草莓、葡萄、樱桃等香味的食用香精.M属于芳香化合物,苯环上只含一个直支链,能发生加聚反应和水解反应.测得M的摩尔质量为162g?mol-1,只含碳、氢、氧三种元素,且原子个数之比为5:5:1.
肉桂酸甲酯M,常用作调制具有草莓、葡萄、樱桃等香味的食用香精.M属于芳香化合物,苯环上只含一个直支链,能发生加聚反应和水解反应.测得M的摩尔质量为162g?mol-1,只含碳、氢、氧三种元素,且原子个数之比为5:5:1.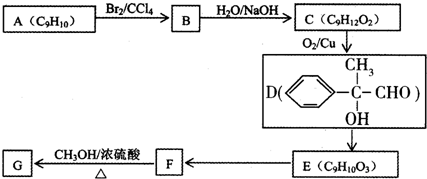
查看答案和解析>>
科目:高中化学 来源: 题型:
 两种有机物A、B的分子式均为C11H12O5,均能发生如图变化.
两种有机物A、B的分子式均为C11H12O5,均能发生如图变化.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、某溶液加AgNO3溶液生成白色沉淀,说明原溶液中有Cl- |
| B、某溶液加BaCl2溶液生成白色沉淀,说明原溶液中有SO42- |
| C、某溶液加NaOH溶液生成蓝色沉淀,说明原溶液中有Cu2+ |
| D、某溶液加KOH溶液生成红褐色沉淀,说明原溶液中有Mg2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
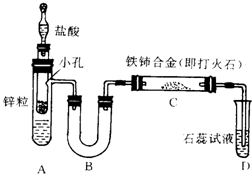 已知亚硝酸铵很不稳定,在溶液中加热能分解生成氮气和水.有人设计以下装置(A中盛有饱和NaNO2与NH4Cl的混合溶液)来进行有关实验.
已知亚硝酸铵很不稳定,在溶液中加热能分解生成氮气和水.有人设计以下装置(A中盛有饱和NaNO2与NH4Cl的混合溶液)来进行有关实验.查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 锂是制造化学和电源的重要原料,如LiFePO4电池某电极的工作原理如图所示,下列有关说法正确的是( )
锂是制造化学和电源的重要原料,如LiFePO4电池某电极的工作原理如图所示,下列有关说法正确的是( )| A、充电时该电极为阴极 |
| B、放电时该电极的反应式为FePO4+e-+Li+=LiFePO4 |
| C、放电时Li+向负极移动 |
| D、该电池可以用硫酸溶液作电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:
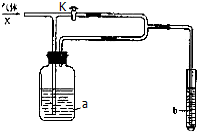 如图装置,在关闭活塞K时通入气体X,b中溶液没有明显现象;开启活塞K通入气体X,则b中溶液有明显现象,下列判断中合理的是( )
如图装置,在关闭活塞K时通入气体X,b中溶液没有明显现象;开启活塞K通入气体X,则b中溶液有明显现象,下列判断中合理的是( )| a中溶液 | b中溶液 | 气体X | |
| A | 饱和食盐水 | KI-淀粉溶液 | Cl2 |
| B | 酸性KMnO4溶液 | 稀品红溶液 | SO2 |
| C | 饱和NaHS溶液 | CuCl2溶液 | HCl |
| D | 饱和NaHCO3溶液 | 石灰水 | CO2 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
 研究硫及其化合物的性质具有重要意义.
研究硫及其化合物的性质具有重要意义.| 第1组 | 第2组 | 第3组 |
| S(单质) | SO2、H2SO3、NaHSO3、Na2SO3 | SO3、X、NaHSO4、Na2SO4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com