
【题目】相对分子质量为M的气态化合物vL(标准状况),溶于mg水中,得到质量分数为w的溶液,物质的量浓度为cmolL﹣1 , 密度为ρgcm﹣3 , 则下列说法不正确的是( )
A.相对分子质量M= ![]()
B.物质的量浓度c= ![]()
C.质量分数w= ![]()
D.溶液密度ρ= ![]()
【答案】C
【解析】解:A.标准状况下vL 气体的物质的量为: ![]() =
= ![]() mol,水的质量分数为1﹣w,该溶液中含有该气体的质量为:
mol,水的质量分数为1﹣w,该溶液中含有该气体的质量为: ![]() ×w=
×w= ![]() g,则该气体的摩尔质量为:M=
g,则该气体的摩尔质量为:M= ![]() =
= ![]() g/mol,该气体的相对分子质量为
g/mol,该气体的相对分子质量为 ![]() ,故A正确;B.该气体的物质的量为
,故A正确;B.该气体的物质的量为 ![]() mol,该气体质量为:
mol,该气体质量为: ![]() mol×Mg/mol=
mol×Mg/mol= ![]() g,所得溶液质量为:mg+
g,所得溶液质量为:mg+ ![]() g,所得溶液的体积为:
g,所得溶液的体积为: ![]() =
= ![]() L,则该溶液的物质的量浓度为:c=
L,则该溶液的物质的量浓度为:c= ![]() =
= ![]() mol/L,故B正确;
mol/L,故B正确;
C.该气体质量为 ![]() g,所得溶液质量为(m+
g,所得溶液质量为(m+ ![]() )g,该溶液的质量分数为w=
)g,该溶液的质量分数为w= 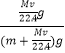 =
= ![]() ,故C错误;
,故C错误;
D.设溶液体积为xcm﹣3 , 该溶液中含有溶质的质量为:Mg/mol×cmol/L×x×10﹣3L=cMx×10﹣3g,该溶液质量为: ![]() ,该溶液的密度为:ρ=
,该溶液的密度为:ρ= ![]() gcm﹣3=
gcm﹣3= ![]() gcm﹣3 , 故D正确;
gcm﹣3 , 故D正确;
故选C.


科目:高中化学 来源: 题型:
【题目】标准状况下,往100mL 0.1mol/L的FeBr2溶液中通入一定体积的Cl2 , 充分反应后,溶液中有50%的Br﹣被氧化.则通入的氯气的体积是( )
A.0.224L
B.0.336L
C.0.448L
D.0.672L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是
A. 氧化还原反应的本质是元素化合价的升降
B. 氧化反应和还原反应必然同时发生
C. 氧化剂在反应中失去电子,所含元素化合价升高,被氧化
D. 还原剂在反应中失去电子,所含元素化合价升高,被还原
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据题意回答问题
(1)常温下,在纯水中加入某一元酸钠盐NaA使溶液的pH=9,则该溶液中水电离出来的C(OH﹣)=molL﹣1 , KW值(填增大、减小或不变).
(2)将锌片与铜片用导线连接插入硫酸铜溶液时,锌片上释放的电子沿流向铜片,阳离子从极到极.不纯的金属或合金与空气中的水溶液接触,发生原电池反应而腐蚀的过程是金属腐蚀的主要形式.当生铁表面的水膜酸性较强时产生腐蚀,其负极的电极反应式为 . 正极的电极反应式为 . 当水膜酸性很弱或呈中性时,正极的电极反应为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.形成离子键的阴阳离子间只存在静电吸引力
B.HF、HCl、HBr、HI的热稳定性和还原性均依次减弱
C.第三周期非金属元素含氧酸的酸性从左到右依次增强
D.元素周期律是元素原子核外电子排布周期性变化的结果
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( ) ①NH3的水溶液能导电,故NH3是电解质
②向含有BaCl2和NaOH的混合溶液中通入少量的二氧化硫气体,有白色沉淀生成
③101kPa、150℃时,agCO和H2的混合气体在足量的O2中完全燃烧,将燃烧后的产物通入足量的Na2O2固体后,Na2O2增重ag
④碱性氧化物一定是金属氧化物
⑤22.4L的CO气体和28g N2所含的电子数相等
⑥根据分散系是否具有丁达尔效应将分散系分为溶液、胶体和浊液
⑦为测定熔融氢氧化钠的导电性,可在瓷坩埚中熔化氢氧化钠固体后进行测量
⑧氧化还原中,有一种元素被氧化,一定有另一种元素被还原.
A.②③④
B.②④⑦⑧
C.①⑤⑥⑦
D.③⑤⑥⑧
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质转化在给定条件下能实现的是( ) ①Al2O3 ![]() NaAlO2(aq)
NaAlO2(aq) ![]() Al(OH)3
Al(OH)3
②S ![]() SO3
SO3 ![]() H2SO4
H2SO4
③NaOH(aq) ![]() NaHCO3
NaHCO3 ![]() Na2CO3
Na2CO3
④Fe ![]() FeCl2
FeCl2 ![]() FeCl3 .
FeCl3 .
A.①③
B.②③
C.②④
D.①④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列转化关系中,X、Y是生活中生活中用途广泛的两种金属单质,A、B是氧化物,A呈红棕色,C、D、E是中学常见的三种化合物.分析转化关系回答问题: 
(1)请写出反应①的化学方程式 .
(2)试剂a是溶液(写一种即可)
(3)若试剂b是H2SO4 , 工业上用E、H2SO4和NaNO2 为原料制取高效净水剂Y(OH)SO4 , 已知还原产物为NO,则该反应的化学方程式是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】完成下列问题. I.已知甲和乙为中学常见金属单质,丙和丁为常见气体单质,A~E为常见化合物;A为淡黄色固体,常温下B为液体,C的焰色反应为黄色.试回答下列问题:
(1)A和 E的化学式分别为、;
(2)A+B→C+丙的化学方程式:;
(3)D+C→B+E的离子方程式:;
(4)1mol甲和1mol乙混合投入足量的B中,在标准状况下最多能产生L丁气体.
(5)II.在标准状况下,取甲、乙、丙各30.mL相同浓度的盐酸,然后分别慢慢加入组成相同的镁铝混合物,得下表中有关数据(反应前后溶液体积不发生变化).
实验序号 | 甲 | 乙 | 丙 |
混合物质量/mg | 255 | 385 | 459 |
气体体积/mL | 280 | 336 | 336 |
①甲组实验中,盐酸(填“过量”“适量”或“不足”);乙组实验中,盐酸(填“过量”“适量”或“不足”)
②盐酸的物质的量浓度为mol/L..
③混合物中Mg和Al的物质的量之比为 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com