
| A. | 氯化铵与Ba(OH)2•8H2O反应 | B. | 钠与冷水反应 | ||
| C. | 锌片与稀硫酸反应 | D. | 铝粉与三氧化二铁的反应 |
分析 A.氯化铵与Ba(OH)2•8H2O反应为吸热反应;
B.钠与冷水反应为放热反应;
C.锌片与稀硫酸反应为放热反应;
D.铝粉与氧化铁的反应为放热反应.
解答 解:A.氢氧化钡晶体与氯化铵晶体混合:Ba(OH)2•8H2O+2NH4Cl═2NH3+BaCl2+10H2O是典型的在常温下反应的吸热反应;
B.钠与冷水反应,生成氢氧化钠和氢气,放出大量的热,是放热反应;
C.锌片与稀硫酸反应生成硫酸锌和氢气,是放热反应;
D.氧化铁和铝在高温的条件下生成氧化铝和铁,Fe2O3+2Al$\frac{\underline{\;高温\;}}{\;}$Al2O3+2Fe,是典型的放热反应,利用放出的热冶炼金属铁,常用于野外铁轨的焊接,为放热反应;
根据以上分析与其它三者不同的是A.
故选A.
点评 本题考查了放热反应和吸热反应,熟记常见的放热反应和吸热反应是解答的关键,题目较简单.


科目:高中化学 来源: 题型:选择题
| 化学键 | H-O | O=O |
| 键能/KJ?mol-1 | 463.4 | 498 |
| A. | 413KJ/mol | B. | 557KJ/mol | C. | 221.6KJ/mol | D. | 436KJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
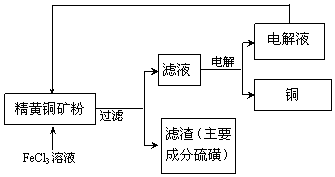
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①⑤ | B. | ②④ | C. | ①②④ | D. | ②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢氧化铁、硝酸、烧碱、氯化钠 | B. | 干冰、碳酸、纯碱、硫酸钾 | ||
| C. | 水、硫酸、熟石灰、氯化钾 | D. | 氨水、醋酸、氢氧化铁、食盐 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 铜作负极 | B. | 锌作正极 | ||
| C. | 电子由铜经导线流向锌 | D. | 锌片上的反应为:Zn-2e-=Zn2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 品名 | 蔬菜苏打饼 |
| 配料 | 面粉、鲜鸡蛋、精炼食用植物油、白砂糖、奶油、食盐、脱水青菜、橙汁 |
| 保质期 | 十二个月 |
| 生产日期 | 2016 年8月20日 |
| A. | 富含蛋白质的是鸡蛋 | |
| B. | 富含维生素的是脱水青菜和橙汁 | |
| C. | 富含糖类的物质只有白砂糖 | |
| D. | 富含油脂的是精炼食用植物油和奶油 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 乙酸乙酯是重要的有机物,某化学兴趣小组对乙酸乙酯的制取进行探究活动.
乙酸乙酯是重要的有机物,某化学兴趣小组对乙酸乙酯的制取进行探究活动.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com