
| A. | 4.0 g重水(D2O)中所含质子数为0.4NA | |
| B. | 4.48 L N2与CO的混合物中所含分子数为0.2NA | |
| C. | 6.2 g白磷与红磷的混合物中所含磷原子数为0.2NA | |
| D. | 12.5 mL 16 mol•L-1浓硫酸与足量铜反应,转移电子数为0.2NA |
分析 A、重水中含有10个质子,重水的摩尔质量为20g/mol;
B、气体所处的状态不明确;
C、白磷与红磷都只含有磷原子;
D、稀硫酸和铜不反应.
解答 解:A、4.0g重水(D2O)的物质的量为0.2mol,0.2mol重水中含有2mol质子,所含质子数为4NA,故A错误;
B、气体所处的状态不明确,故4.48L气体的物质的量不明确,故含有的分子个数不能计算,故B错误;
C、白磷和红磷都是P原子形成的不同单质,则6.2 g白磷与红磷的混合物中所含磷原子的物质的量是6.2g÷31g/mol=0.2mol,则原子数为0.2×6.02×1023,故C正确;
D、在浓硫酸和铜的反应中,由于随着反应的进行,浓硫酸的浓度逐渐降低,而稀硫酸和铜不反应,因此实际转移电子的个数小于0.2×6.02×1023,故D错误.
故选C.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 1mol有机物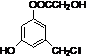 分别能与1molNa2CO3、2molNa、3molBr2、4molNaOH反应 分别能与1molNa2CO3、2molNa、3molBr2、4molNaOH反应 | |
| B. | 有机物分子 与银氨溶液作用后仍具有光学活性 与银氨溶液作用后仍具有光学活性 | |
| C. | 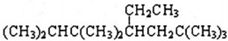 的正确命名为2,3,3,6,6-五甲基-4-乙基庚烷 的正确命名为2,3,3,6,6-五甲基-4-乙基庚烷 | |
| D. | 2-甲基-1,3-丁二烯在一定温度下和Br2按物质的量之比1:1发生加成反应,所得产物主要有三种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO2的电子式 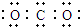 | B. | Cl-的结构示意图 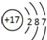 | ||
| C. | HCl的电子式 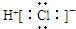 | D. | 质量数为37的氯原子${\;}_{17}^{37}$Cl |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 ,F元素原子的电子排布式1s22s22p63s23p5,
,F元素原子的电子排布式1s22s22p63s23p5,查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若完全燃烧,1 mol雌酮(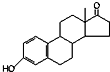 )比雄酮( )比雄酮(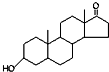 )多消耗3 mol O2 )多消耗3 mol O2 | |
| B. | 正戊烷、异戊烷和新戊烷互为同分异构体,沸点依次升高 | |
| C. | 甲醛、甲酸、甲酸钠,均能发生银镜反应 | |
| D. | 乙醇依次通过消去、取代、加成反应可生成乙二醇 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com