
���� ��n��Cu��=$\frac{32g}{64g/mol}$=0.5mol��������������ʵ���=$\frac{11.2L}{22.4L/mol}$=0.5mol������Nԭ���غ����������������������ʵ��������������ƵĻ�ѧʽ�����������õ����ᣬ�ٸ������ʵ���Ũ�ȹ�ʽ������������ʵ���Ũ�ȣ�
����ʹͭ�����ᷴӦ���ɵ�������NaOH��Һ��ȫ��ת��ΪNaNO3����ϵ�ʧ�����غ�������㣮
��� �⣺��n��Cu��=$\frac{32g}{64g/mol}$=0.5mol��������������ʵ���=$\frac{11.2L}{22.4L/mol}$=0.5mol����ͭ����ȫ��ת���ɳ���ʱͬʱ���������ƣ�������ԭ���غ��n��NaOH��=n��NaNO3��=0.001aVmol����������������غ���������õ���������ʵ���=0.001aVmol������Nԭ���غ�������������������ʵ���=0.5mol��������������ʵ���Ũ��=$\frac{0.5mol+0.001aVmol}{0.14L}$=$\frac{50+0.1aV}{14}$mol/L��
�ʴ�Ϊ��$\frac{50+0.1aV}{14}$mol/L��
������Ҫ˫��ˮmg�����ݵ��ӵ�ʧ�غ㣬��˫��ˮ�õ��ĵ��Ӽ�ͭʧȥ�ĵ��ӣ������У�0.5��2=$\frac{m}{34}$��2����ã�m=17���ʴ�Ϊ��17��
���� ����������Ϊ���忼����������ԭ��Ӧ�ļ��㣬����������ԭ��Ӧ�е�ʧ���ӽ��н�ɣ�ע���غ�˼������ã�ע����в��ܸ���ͭ����������������ʵ�����ͭ�����ᷴӦʱ�����������ʣ�࣬Ϊ�״��㣮


 ������ҵ��ٳɳ����½������������ϵ�д�
������ҵ��ٳɳ����½������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �Ͻ�����ĸ��ɷֽ������۵�ͣ�Ӳ�ȴ� | |
| B�� | �����ֶ������ĺϽ���Ҫ�ɷֶ����������IJ�ͬ�Ǻ�̼�� | |
| C�� | �������ȷ�Ӧԭ�����������۵�ϸߵĽ����� | |
| D�� | ���Բ��õ���Ȼ�����Һ�ķ����Ƶý����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | CH3CH2OH | B�� | CH3CH2CH2OH | C�� | CH3OH | D�� | CH3-O-CH3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
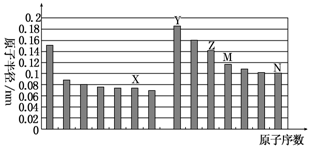
| A�� | X��N����Ԫ�ص���̬�⻯��ķе���ȣ�ǰ�߽ϵ� | |
| B�� | Z���������ֱܷ��ܽ���Y�����������N���⻯���ˮ��Һ | |
| C�� | ��X��M����Ԫ����ɵĻ����ﲻ�����κ��ᷴӦ��������ǿ�Ӧ | |
| D�� | Z��N����Ԫ�ص����Ӱ뾶��ȣ�ǰ�߽ϴ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��صĵ��Һ��ΪLiClˮ��Һ | |
| B�� | �ŵ�ʱ������ӦʽΪ��Li-e-+Cl-=LiCl | |
| C�� | �ŵ�ʱ������ӦʽΪ��2SOCl2+4e-=4Cl-+S+SO2 | |
| D�� | �ŵ�ʱ���ӴӸ��������·�����������ٴ���������������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 7.8gNa2O2������������0.2 NA | |
| B�� | ���³�ѹ�£�8 g O2���еĵ�������4NA | |
| C�� | ��״���£�2.24 L CCl4�к��еķ�����Ϊ0.1NA | |
| D�� | 1 L 1.0 mol•L-1Na2CO3��Һ�к��е���ԭ����Ϊ3NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | NH3 | B�� | CO | C�� | H2S | D�� | SO2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com