
分析 (1)新制氢氧化铜浊液需要氢氧化钠溶液过量,在碱性溶液中才会和醛基反应生成氧化亚铜红色沉淀;
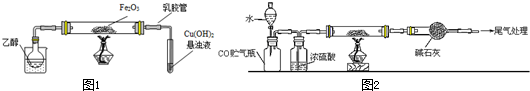
(2)依据图1装置分析可知,乙醇易挥发,可以对烧杯加热或烧杯中加入热水;阻止倒吸的操作是迅速拆下导气管;
(3)依据反应现象可知,乙醇蒸气在氧化铁做催化剂作用下生成乙醛,试管内发生的是乙醛和氢氧化铜加热反应生成红色氧化亚铜沉淀;
(4)依据铁离子的实验检验方法分析,铁离子加入硫氰酸钾溶液会变红色;乙醇和氧化铁反应过程中可能会生成铁或四氧化三铁,能被磁铁吸引;
(5)实验过程依据反应原理和实验目的分析实验步骤为,组装装置,检验装置气密性,加入试剂,加入水吧一氧化碳赶入后续装置,点燃酒精灯加热玻璃管,反应结束后停止加热,关闭分液漏斗活塞,玻璃管称量剩余固体,依据质量变化计算铁元素和氧元素物质的量之比;
(6)依据实验结果得到,碱石灰增重mg,即二氧化碳的质量为mg,则铁的氧化物中减少的质量为氧元素的质量为$\frac{16}{44}$mg=$\frac{4}{11}$mg,铁的质量为(a-$\frac{4}{11}$m)g,依据元素物质的量计算得到比值.
解答 解:(1)新制氢氧化铜浊液需要氢氧化钠溶液过量,在碱性溶液中才会和醛基反应生成氧化亚铜红色沉淀,制备过程为在过量NaOH溶液中滴加数滴CuSO4溶液,
故答案为:在过量NaOH溶液中滴加数滴CuSO4溶液;
(2)依据图1装置分析可知,乙醇易挥发,可以对烧杯加热或烧杯中加入热水;阻止倒吸的操作是迅速拆下导气管,
故答案为:在烧杯中加入热水(对烧杯加热);c;
(3)依据反应现象可知,乙醇蒸气在氧化铁做催化剂作用下生成乙醛,试管内发生的是乙醛和氢氧化铜加热反应生成红色氧化亚铜沉淀,反应的化学方程式为:CH3CHO+2Cu(OH)2 $\stackrel{△}{→}$Cu2O↓+CH3COOH+2H2O;
故答案为:CH3CHO+2Cu(OH)2 $\stackrel{△}{→}$Cu2O↓+CH3COOH+2H2O;
(4)依据铁离子的实验检验方法分析,铁离子加入硫氰酸钾溶液会变红色,取少量溶液加入KSCN溶液,变红色,则有Fe3+;氧化铁做催化剂参与反应过程,乙醇和氧化铁反应过程中可能会生成铁或四氧化三铁,能被磁铁吸引;
故答案为:取少量溶液加入KSCN溶液,变红色,则有Fe3+;b;
(5)实验过程依据反应原理和实验目的分析实验步骤为,组装装置,检验装置气密性,加入试剂,加入水把一氧化碳赶入后续装置,点燃酒精灯加热玻璃管,反应结束后停止加热,关闭分液漏斗活塞,玻璃管称量剩余固体,依据质量变化计算铁元素和氧元素物质的量之比,所以选c,
故答案为:c;
(6)依据实验结果得到,碱石灰增重mg,即二氧化碳的质量为mg,则铁的氧化物中减少的质量为氧元素的质量为$\frac{16}{44}$mg=$\frac{4}{11}$mg,铁的质量为(a-$\frac{4}{11}$m)g,依据元素物质的量计算得到比值,n(Fe):n(O)=(a-$\frac{4}{11}$m):$\frac{4}{11}$m=$\frac{11a-4m}{4m}$,
故答案为:$\frac{11a-4m}{4m}$.
点评 本题考查了物质性质的实验探究和物质组成的分析判断,实验操作步骤的设计和完善,实验过程中的反应实质分析判断,现象的理解和应用是解题关键,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 金属冶炼的本质是将化合态金属还原为游离态,冶炼方法由金属的活泼性决定 | |
| B. | Cu的湿法冶炼是将金属钠投入到CuSO4溶液中置换出铜 | |
| C. | 炼铁时加入石灰石的目的是除去过量的碳 | |
| D. | 由于Al的活泼性强,故工业上采用电解熔融AlCl3的方法生产Al |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 晶体硅的导电性介于金属和绝缘体之间,是良好的半导体 | |
| B. | 加热到一定温度时,硅能与氯气、氧气等非金属反应 | |
| C. | 利用二氧化硅与C反应能制得粗硅 | |
| D. | 二氧化硅性质较稳定,常温下不与任何物质反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3Fe+4H2O$\frac{\underline{\;高温\;}}{\;}$Fe3O4+4H2 | B. | 3NO2+H2O═2HNO3+NO | ||
| C. | 2Na2O2+2H2O═4NaOH+O2↑ | D. | 2F2+2H2O═4HF+O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 天津8.12爆炸事件中,港口保存有NaCN等剧毒物品.
天津8.12爆炸事件中,港口保存有NaCN等剧毒物品.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
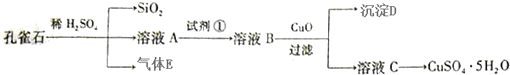
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
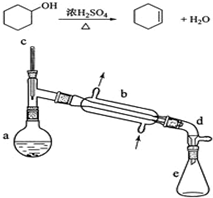 醇脱水是合成烯烃的常用方法,实验室合成环己烯的反应和实验装置如下:
醇脱水是合成烯烃的常用方法,实验室合成环己烯的反应和实验装置如下:| 相对分子质量 | 密度(g/cm3) | 沸点/℃ | 溶解性 | |
| 环己醇 | 100 | 0.9618 | 161 | 微溶于水 |
| 环己烯 | 82 | 0.8102 | 83 | 难溶于水 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com