
少量铁粉与100mL 0.01mol/L的稀盐酸反应,反应速率太慢.为了加快此反应速率可以使用如下方法( )
A. 加H2O B. 加入饱和食盐水
C. 增大压强 D. 升高温度(不考虑盐酸挥发)
 一诺书业暑假作业快乐假期云南美术出版社系列答案
一诺书业暑假作业快乐假期云南美术出版社系列答案科目:高中化学 来源: 题型:
合成氨反应:N2(g)+3H2(g)
 2NH3(g)
2NH3(g)
ΔH=-92.4kJ·mol-1,在反应过程中,正反应速率的变化如下图:

下列说法正确的是( )
A.t1时升高了温度B.t2时使用了催化剂
C.t3时增大了压强D.t4时降低了温度
查看答案和解析>>
科目:高中化学 来源: 题型:
对于反应2SO2(g)+O2(g)2SO3(g),能增大正反应速率的措施是( )
A.通入大量O2 B.增大容器容积 C.移去部分SO3 D.降低体系温度
查看答案和解析>>
科目:高中化学 来源: 题型:
水溶液中能大量共存的一组离子是( )
A. K+、NH4+、OH﹣、SO42﹣ B. H+、Fe2+、SO42﹣、ClO﹣
C. Na+、Ca2+、Cl﹣、CO32﹣ D. K+、Ca2+、Cl﹣、NO3﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
汽车尾气里含有有毒的NO和CO,NO和CO能缓慢地反应生成N2和CO2.对此反应的下列叙述不正确的是( )
A. 使用催化剂能加快反应速率
B. 升高温度能加快反应速率
C. 改变压强对反应速率无影响
D. 此反应能减轻尾气对环境的污染
查看答案和解析>>
科目:高中化学 来源: 题型:
)某班学生分成甲,乙两小组分别探究硫,氮及其化合物的性质:
(一)甲组同学用图1装置来探究浓硫酸与木炭粉加热反应并验证反应所产生的各种产物.
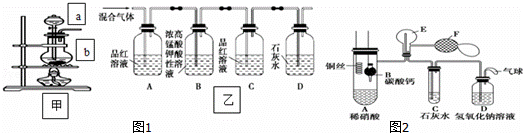
(1)装置甲中盛放浓硫酸的仪器a名称是 ,装置甲中仪器b中发生反应的化学方程式为
(2)实验中可观察到装置乙中,A瓶的溶液褪色,C瓶的溶液不褪色.
A瓶溶液的作用是 ,
D瓶溶液的现象是 .
(二)乙组同学用图2装置来证明铜与稀硝酸反应产生一氧化氮,B为一个用金属丝固定的干燥管,内装块状碳酸钙固体;E为一个空的蒸馏烧瓶;F是用于鼓入空气的双连打气球.(1)实验时,先将B装置下移,使碳酸钙与稀硝酸接触产生气体,当C处产生白色沉淀时,立刻将B装置上提,使之与稀硝酸分离.该组学生设计此步操作的目的是 .
(2)装置E中开始时出现浅红棕色气体,用F向E中鼓入空气后,可观察到烧瓶E内气体颜色加深,产生上述现象的原因是 .
(3)一段时间后,C中白色沉淀溶解,其原因是
(4)装置D的作用是
查看答案和解析>>
科目:高中化学 来源: 题型:
黑火药爆炸时可发生如下反应:5S+16KNO3+16C=3K2SO4+4K2CO3+K2S+12CO2↑+8N2↑,下列有关说法正确的是( )
A. S既作氧化剂又作还原剂
B. 消耗12gC时,反应转移5mol电子
C. 还原产物只有K2S
D. KNO3只发生氧化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
溶液、胶体和浊液这三种分散系的根本区别是( )
A.是否是大量分子或离子的集合体
B.分散质粒子的大小
C.是否能通过滤纸
D.是否均一、透明、稳定
查看答案和解析>>
科目:高中化学 来源: 题型:
ClO2是一种广谱型的消毒剂,根据世界环保联盟的要求,ClO2将逐渐取代Cl2成为生产自来水的消毒剂.工业上ClO2常用NaClO3和Na2SO3溶液混合并加H2SO4酸化后反应制得,其中Na2SO3被氧化为Na2SO4.在以上反应中,NaClO3和Na2SO3的物质的量之比为( )
|
| A. | 1:1 | B. | 2:1 | C. | 1:2 | D. | 2:3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com