


 快乐暑假暑假能力自测中西书局系列答案
快乐暑假暑假能力自测中西书局系列答案科目:高中化学 来源: 题型:
| A、pH=0的溶液. |
| B、0.03 mol?L-1 H2SO4. |
| C、0.05 mol?L-1 HClO |
| D、0.05 mol?L-1的NaHSO4. |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、分子是不断运动的 |
| B、分子能保持物质的化学性质 |
| C、分子之间有间隙 |
| D、分子是由原子构成的 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、262.6 kJ?mol-1 |
| B、-131.3 kJ?mol-1 |
| C、-352.3 kJ?mol-1 |
| D、131.3 kJ?mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
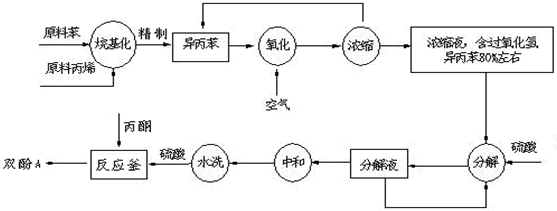
 (2)在氧化操作中,需要严格控制温度,防止温度过高.其原因是:①防止反应过于剧烈②
(2)在氧化操作中,需要严格控制温度,防止温度过高.其原因是:①防止反应过于剧烈②查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NH4Cl |
| B、NaOH |
| C、Na2CO3 |
| D、Fe |
查看答案和解析>>
科目:高中化学 来源: 题型:
压强/MPa 体积分数/% 温度/℃ | 1.0 | 2.0 | 3.0 |
| 810 | 54.0 | a | b |
| 915 | c | 75.0 | d |
| 1000 | e | f | 83.0 |
| A、b>f |
| B、K(1000℃)>K(810℃) |
| C、915℃、2.0MPa时E的转化率为60% |
| D、该反应的△S>0 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com