
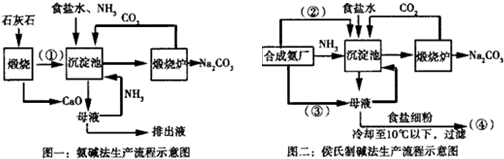
���� ��1�����������̼������ɶ�����̼�������Ƽ�У���ʳ��ˮ����ͨ�백������ͨ�������̼����Ӧ����̼�����ƺ��Ȼ�泥�����̼�����ƾ����ĸҺ�к����Ȼ�泥���ĸҺ�м����Ȼ�����ȴ�õ��Ȼ�茶��壻
��2���������ʳ�Σ��Ȼ��ƣ���ʯ��ʯ��������������ʯ�ҺͶ�����̼��������Ϊԭ������ȡ��������в�������CaCl2�Ļ�ѧ����ʽΪ��2NH4Cl+Ca��OH��2$\frac{\underline{\;\;��\;\;}}{\;}$2NH3��+CaCl2+2H2O���������Ƽ���У���ĸҺ��ͨ�백������������Һ��笠����ӵ�Ũ�ȣ�
��3�������Ƽ��CO2��Դ��ʯ��ʯ���գ������CO2����Դ�ںϳɰ���ҵ�ķ�����
��4���÷�̪��ָʾ���ζ�ʱ�������ķ�ӦΪNa2CO3+HCl=NaHCO3+NaCl���������ĵ����������Ӧ��̼���Ƶ����ʵ�������������������������������
��� �⣺��1�����������̼������ɶ�����̼�����Ԣ�ΪCO2�������Ƽ�У���ʳ��ˮ����ͨ�백������ͨ�������̼����Ӧ����̼�����ƺ��Ȼ�泥�����̼�����ƾ����ĸҺ�к����Ȼ�泥���ĸҺ�м����Ȼ�����ȴ�õ��Ȼ�茶��壬���Ժ����Ƽ����ͼ�У���CO2����CO2����NH3����NH4Cl��
�ʴ�Ϊ��CO2��CO2��NH3��NH4Cl��
��2����������в�������CaCl2�����Ȼ�狀���ʯ���ڼ��������·�Ӧ�����ɰ������Ȼ��Ƶķ�Ӧ����Ӧ�Ļ�ѧ����ʽΪ2NH4Cl+Ca��OH��2$\frac{\underline{\;\;��\;\;}}{\;}$2NH3��+CaCl2+2H2O���������Ƽ���У���ĸҺ�к����Ȼ�泥���ĸҺ��ͨ�백������������Һ��笠����ӵ�Ũ�ȣ�ʹNH4Cl�Ծ������ʽ������
�ʴ�Ϊ��2NH4Cl+Ca��OH��2$\frac{\underline{\;\;��\;\;}}{\;}$2NH3��+CaCl2+2H2O������NH4+��Ũ�ȣ�������NH4Cl����������
��3��CO2���Ƽҵ����Ҫԭ�ϣ������Ƽ��CO2��Դ�ںϳɰ���ҵ�ķ����������CO2����Դ��ʯ��ʯ���գ�ʯ��ʯ��Ҫ�ɷ���̼��ƣ�̼����ڸ����·ֽ����ɶ�����̼�������ƣ�
�ʴ�Ϊ���������CO2��Դ��ʯ��ʯ���գ��������Ƽ��CO2��Դ�ںϳɰ���ҵ�ķ�����
��4���÷�̪��ָʾ���ζ�ʱ�������ķ�ӦΪNa2CO3+HCl=NaHCO3+NaCl��
��n��Na2CO3��=0.1000mol/L��0.025L��$\frac{250mL}{25mL}$=0.1mol��
m��Na2CO3��=nM=0.1mol��106g/mol=10.6g��
��Ʒ�д��������������$\frac{10.6g}{11g}$��100%=96.4%��
�ʴ�Ϊ��96.4%��
���� ���⿼��������Ͱ���������̵�ԭ���ȽϺ����ʷ����жϣ���Ŀ�Ѷ��еȣ���ȷ������Ӧԭ��Ϊ���ؼ���ע�����հ���ͺ����Ƽ��ԭ�����豸��֪ʶ������������ѧ�������Ӧ��������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | VA=0.15 mol•L-1•min-1 | B�� | VC=0.6 mol•L-1•min-1 | ||
| C�� | VB=0.6 mol•L-1•min-1 | D�� | VD=0.1 mol•L-1•min-1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ������ | Fe3+ | Fe2+ | Cu2+ |
| ��ʼ����ʱ��pH | 1.9 | 7.0 | 4.7 |
| ������ȫʱ��pH | 3.2 | 9.0 | 6.7 |
| A�� | �ں���Fe2+��Fe3+��Cu2+�Ļ����Һ�У��μ�����������ҺʱFe2+�Ȳ������� | |
| B�� | �ں���Fe2+��Fe3+��Cu2+�Ļ����Һ�У�����ȥ�����Һ�е�Fe2+��Fe3+�����ȼ���ϡ���ᣬ�ټ�������ͭ������Һ��pH�ķ�ΧΪ3.2-4.7 | |
| C�� | ��ͬ�¶��£�Ksp[��Cu��OH��2����Ksp[��Fe��OH��2�� | |
| D�� | �ں���Fe2+��Fe3+��Cu2+�Ļ����Һ�У���ȥ�����Һ�е�Fe2+��Fe3+���ɼ������������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����������������䣬˵����Ӧ�Ѵ�ƽ��״̬ | |
| B�� | ��С������������´ﵽƽ��ʱ������������C%�������� | |
| C�� | �ں�ѹ�����������¶ȣ�����������C%������������С | |
| D�� | �ں��������������¶ȣ��ﵽ��ƽ��ʱ��������ܶ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Fe3+ | B�� | Cr3+ | C�� | Zn2+ | D�� | Mg2+ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
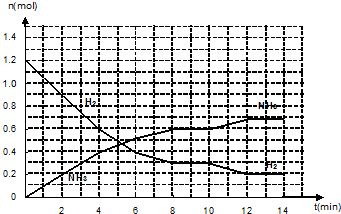
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
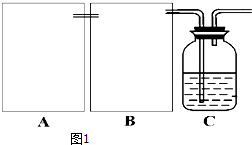
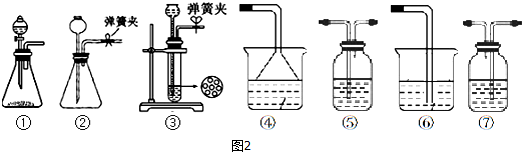
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| ��� | �����Ƽ | ||
| A�� | ԭ�� | ʳ�Ρ���������ʯ�� | ʳ�Ρ�������������̼ |
| B�� | ������ | �Ȼ��� | �Ȼ�� |
| C�� | ѭ������ | ������������̼ | �Ȼ��� |
| D�� | ���� | ԭ���ã��豸���ӣ��ܺĸ� | ԭ�������ʸߣ��������� |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
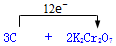 ��
���鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com