
| A. | C4H10 | B. | C4H4Cl2 | C. | CH2Cl2 | D. | C5H12 |
分析 同分异构体是分子式相同,但结构不同的化合物,根据是否存在同分异构体判断正误;
解答 解:A.C4H10存在2种同分异构体:CH3CH2CH2CH3、CH3CH(CH3)CH3,所以不能只表示一种物质,故A错误;
B.C4H4Cl2同的不饱和度为2,可以含有2个双键或1个三键或1个双键、1个环,具有同分异构体,所以不能只表示一种物质,故B错误;
C.CH2Cl2只有一种结构不存在同分异构体,所以能只表示一种物质,故C正确;
D.C5H12存在3种同分异构体:CH3-CH2-CH2-CH2-CH3、 、
、 ,所以不能只表示一种物质,故D错误;
,所以不能只表示一种物质,故D错误;
故选C.
点评 本题考查常见有机化合物的结构,题目难度中等,注意CH2Cl2只代表一种物质.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | 84g | B. | 32g | C. | 87g | D. | 197g |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 装置 | 药品 | 现象 | |
| 实验1 |  | 0.64g Cu片(0.01mol)和20.0mL浓HNO3 | Cu片消失,得到绿色溶液A,放置较长时间后得到蓝色溶液B,… |
| 操作 | 现象 | |
| 实验3 | i.配制与溶液A的c(H+)相同的HNO3溶液,取20.0mL,通入NO2气体 | 溶液呈黄色 |
| ii.再加0.01mol Cu(NO3)2固体搅拌至完全溶解 | 溶液变为绿色 | |
| 3、加水稀释 | 溶液立即变为蓝色 | |
| 实验4 | i.向20.0mL 0.5mol/L Cu(NO3)2蓝色溶液中通入少量NO2 | 溶液呈绿色 |
| ii.加入稀H2SO4 | 有无色气体放出,遇空气变红棕色,溶液很快变为蓝色 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
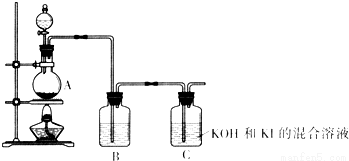
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 当消耗0.1 mol Zn时,得到的还原产物为0.1 mol | |
| B. | 当溶液中不再产生气泡时,溶液中大量存在的阳离子是Zn2+ | |
| C. | 当有第三种单质生成时,消耗的锌粉质量至少大于13 g | |
| D. | 反应结束时,可得到0.25 mol ZnSO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 所有铵盐受热均可分解,产物均有NH3 | |
| B. | 所有铵盐都易溶于水,不是所有铵盐中的氮都呈-3价 | |
| C. | NH4Cl溶液中加入NaOH浓溶液供热,反应的离子方程式为NH4+OH-$\frac{\underline{\;加热\;}}{\;}$NH3↑+H2O | |
| D. | NH4Cl和NaCl的固体混合物可用加热法分离 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com