
| A�� | ����MnO2��H2SO4���������� | B�� | �����ڸ������п�ѭ��ʹ�� | ||
| C�� | ��������16gSʱת��1mol���� | D�� | ����MnSO4����������Ӧ |
���� A��MnO2��MnԪ�صĻ��ϼ۽��ͣ�H2SO4�и�Ԫ�صĻ��ϼ۲��䣻
B���ɣ�1������3����֪������Ȳμӷ�Ӧ���ִӷ�Ӧ�����ɣ�
C����Ӧ��SԪ����-2������Ϊ0��
D��MnԪ�صĻ��ϼ����ߣ�
��� �⣺A��MnO2��MnԪ�صĻ��ϼ۽��ͣ�H2SO4�и�Ԫ�صĻ��ϼ۲��䣬��MnO2����������H2SO4������������ֻ���ᣬ��Aѡ��
B���ɣ�1������3����֪������Ȳμӷ�Ӧ���ִӷ�Ӧ�����ɣ����������������п�ѭ��ʹ�ã���B��ѡ��
C����Ӧ��SԪ����-2������Ϊ0����ÿ����16gS������ת��$\frac{16g}{32g/mol}$����2-0��=1mol���ӣ���C��ѡ��
D��MnԪ�صĻ��ϼ����ߣ�����MnSO4����������Ӧ����D��ѡ��
��ѡA��
���� ���⿼�������ұ����������ԭ��Ӧ����ȷԪ�صĻ��ϼ۱仯�ǽ����Ĺؼ�������Ϥ������ԭ��Ӧ�еĸ����������Ŀ�ѶȲ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
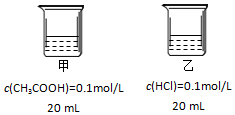
| A�� | �ס������ձ���ˮ�������H+Ũ�ȣ��ף��� | |
| B�� | �ֱ�ϡ����ͬ��������ҺpH�仯����=�� | |
| C�� | ��ͬ�����£�AgCl��s���ڼ����ܽ�ȴ��������� | |
| D�� | ����ձ�����NaOHʹ��Һ���Ժ�һ�����ڣ�c��Na+��=c��CH3COO-��+c��CH3COOH�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �٢� | B�� | �ۢ� | C�� | �ڢ� | D�� | �ڢܢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1 mol CO2 ������Ϊ44g/mol | |
| B�� | CO2��Ħ������Ϊ44g | |
| C�� | 1 mol CO2��������CO2����Է�����������ֵ����ͬ | |
| D�� | CO2��Ħ����������CO2����Է������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ϩ�ĵ���ʽΪ  | B�� | ��ϩ�����ģ��Ϊ 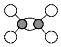 | ||
| C�� | ��ϩ������ƽ��ṹ | D�� | ��ϩ�Ľṹ��ʽΪCH2CH2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Al2O3�۵�ߣ������������������� | |
| B�� | ������ˮ�뽺��������й� | |
| C�� | ����ˮʯ�������ⲻ�ϡ���������ѧ�仯 | |
| D�� | ������������ҹ�족���������ɫ��Ӧ�й� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | HCO3-+H2O=H2CO3+OH- | |
| B�� | HSO3-+H2O?SO32-+H3O+ | |
| C�� | ���ڵ�NaHSO4���룺NaHSO4=Na++HSO4- | |
| D�� | Al��OH��3=H++AlO2-+H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com