
·ÖĪö £Ø1£©×é×°ŅĒĘ÷µÄŅ»°ćĖ³ŠņŹĒ²ÉÓĆĻČĻĀŗóÉĻ£¬ĻČ×óŗóÓŅµÄŌŌņ£¬ĄūÓƱ¾¹ęŌņ¼“æɽā“š£»
£Ø2£©¼ÓČėĀČ»Æ±µČÜŅŗ¼ģŃéĮņĖįøłĄė×ÓŹĒ·ń³ż¾”£»
£Ø3£©ÓÉĮ÷³ĢæÉÖŖ£¬¢ŚÖŠ¼ÓĀČ»Æ±µæɳżČ„ĮņĖįøłĄė×Ó£¬¢ŪÖŠ¼ÓNaOH³żČ„Ć¾Ąė×Ó£¬¢ÜÖŠ¼ÓĢ¼ĖįÄĘæɳżČ„±µĄė×Ó”¢øĘĄė×Ó£¬¹żĀĖŗóÖ÷ŅŖĪŖĀČ»ÆÄĘŗĶĢ¼ĖįÄĘ£¬¢ŽÖŠ¼ÓŃĪĖį·“Ó¦ŗóČÜŅŗÖŠČÜÖŹĪŖNaCl£¬Č»ŗóÕō·¢½į¾§µĆµ½NaCl£®
½ā“š ½ā£ŗ£Ø1£©×é×°ŅĒĘ÷Ź±ŅŖ“ÓĻĀĻņÉĻ×é×°£¬¾Ę¾«µĘŌŚĢśČ¦ŗĶÕō·¢ĆóµÄĻĀ·½£¬ĖłŅŌŅŖĻČ·Å¾Ę¾«µĘ£»Č»ŗóŌŁ¹Ģ¶ØĢśČ¦£¬·ÅÖĆÕō·¢Ćó£»Č»ŗóŌŁµćČ¼¾Ę¾«µĘ¼ÓČČ£¬²¢½Į°č£¬µ±ÓŠ½Ļ¶ą¾§ĢåĪö³öŹ±£¬Ķ£Ö¹¼ÓČČ£¬ĄūÓĆÓąČČÕōøÉ£¬ĖłŅŌÕżČ·µÄ²Ł×÷Ė³ŠņĪŖ£ŗ¢Ū¢Ł¢Ś¢Ü¢Ż£¬
¹Ź“š°øĪŖ£ŗ¢Ū¢Ł¢Ś¢Ü¢Ż£»
£Ø2£©¼ÓČė¹żĮæĀČ»Æ±µČÜŅŗ³żČ„ĮņĖįøłĄė×Ó£¬¼ģŃéĮņĖįøłĄė×ÓŅŃ³ż¾”£¬æÉȔɣĮæČÜŅŗÓŚŹĒŹŌ¹ÜÖŠ¼ÓČėŃĪĖįĖį»ÆµÄBaCl2ČÜŅŗ£¬ČōÓŠ°×É«³Įµķ£¬ŌņÖ¤Ć÷ÓŠSO42-
£»Čē¹ū»¹ÓŠĮņĖįøłĄė×Óƻӊ³ż¾”£¬æÉŅŌŌŚČÜŅŗÖŠ¼ĢŠų¼ÓČė¹żĮæµÄĀČ»Æ±µ£¬·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖBa2++SO42-ØTBaSO4”ż£¬
¹Ź“š°øĪŖ£ŗȔɣĮæČÜŅŗÓŚŹĒŹŌ¹ÜÖŠ¼ÓČėŃĪĖįĖį»ÆµÄBaCl2ČÜŅŗ£¬ČōÓŠ°×É«³Įµķ£¬ŌņÖ¤Ć÷ÓŠSO42-£»¼ÓČėÉŌĪ¢¹żĮæµÄBaCl2ČÜŅŗ£»Ba2++SO42-ØTBaSO4”ż£»
£Ø3£©¢ÜÖŠ¼ÓĢ¼ĖįÄĘæɳżČ„±µĄė×Ó”¢øĘĄė×Ó£¬·¢ÉśĄė×Ó·“Ó¦ĪŖCa2++CO32-ØTCaCO3”ż”¢Ba2++CO32-ØTBaCO3”ż£¬¹Ź“š°øĪŖ£ŗCa2++CO32-ØTCaCO3”ż£»Ba2++CO32-ØTBaCO3”ż£»µŚ¢Ž²½ÖŠ¼ÓČėŃĪĖįµÄÄæµÄŹĒ³żČ„¹żĮæµÄĒāŃõ»ÆÄĘŗĶĢ¼ĖįÄĘ£¬
¹Ź“š°øĪŖ£ŗCa2++CO32-ØTCaCO3”ż£»Ba2++CO32-ØTBaCO3”ż£»³żČ„¹żĮæµÄNaOHČÜŅŗŗĶNa2CO3ČÜŅŗ£®
µćĘĄ ±¾Ģāæ¼²éĪļÖŹ·ÖĄė”¢Ģį“æŹµŃé·½°øµÄÉč¼Ę£¬°ŃĪÕ“ÖŃĪĢį“æĮ÷³ĢÖŠµÄ·ÖĄė·½·Ø¼°·¢ÉśµÄĄė×Ó·“Ó¦ĪŖ½ā“šµÄ¹Ų¼ü£¬²ąÖŲ·ÖĪöÄÜĮ¦¼°ĪļÖŹ³żŌÓµÄ漲飬ĢāÄæÄŃ¶Č²»“ó£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | $\frac{1000wd}{M£Øw+1000£©}$ mol•L-1 | B£® | $\frac{wd}{Mw+1000}$mol•L-1 | ||
| C£® | $\frac{w}{M}$mol•L-1 | D£® | $\frac{1000wd}{wM+1000}$ mol•L-1 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | NaBiO3 | B£® | Na4XeO6 | C£® | K2S2O8 | D£® | PbO2 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
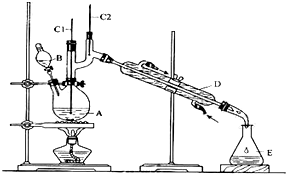
| ·Šµć/”ę | ĆܶČ/£Øg•cm-3£© | Ė®ÖŠČܽāŠŌ | |
| Õż¶”“¼ | 11.72 | 0.8109 | Ī¢ČÜ |
| Õż¶”Č© | 75.7 | 0.8017 | Ī¢ČÜ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
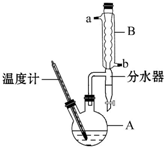 1-äå±ūĶé³£ÓĆ×÷ÓŠ»ś·“Ó¦µÄČܼĮ£®ŹµŃéŹŅÖʱø1-äå±ūĶé£ØCH3CH2CH2Br£©µÄ·“Ó¦ŗĶÖ÷ŅŖŹµŃé×°ÖĆČēĶ¼£ŗ
1-äå±ūĶé³£ÓĆ×÷ÓŠ»ś·“Ó¦µÄČܼĮ£®ŹµŃéŹŅÖʱø1-äå±ūĶé£ØCH3CH2CH2Br£©µÄ·“Ó¦ŗĶÖ÷ŅŖŹµŃé×°ÖĆČēĶ¼£ŗ| Ļą¶Ō·Ö ×ÓÖŹĮæ | ĆÜ¶Č /g•mL-1 | ·Šµć/”ę | Ė®ÖŠ ČܽāŠŌ | |
| Õż±ū“¼ | 60 | 0.896 | 97.1 | ČÜ |
| Õż±ūĆŃ | 102 | 0.74 | 90 | ¼øŗõ²»ČÜ |
| 1-äå±ūĶé | 123 | 1.36 | 71 | ²»ČÜ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
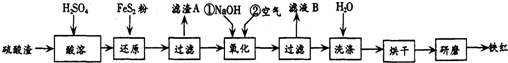
| ³ĮµķĪļ | Fe£ØOH£©3 | Al£ØOH£©3 | Fe£ØOH£©2 | Mg£ØOH£©2 |
| æŖŹ¼³ĮµķpH | 2.7 | 3.8 | 7.6 | 9.4 |
| ĶźČ«³ĮµķpH | 3.2 | 5.2 | 9.7 | 12.4 |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com