
【题目】元素周期表中第VIIA族元素的单质及其化合物的用途广泛.完成下列填空:
(1)与氯元素同族的短周期元素的原子核外有___种不同能量的电子.
(2)能作为溴、碘元素非金属性(原子得电子能力)递变规律的判断依据是___(填序号).
a.IBr中溴为﹣1价 b.HBr、HI的酸性c.HBr、HI的热稳定性 d.Br2、I2的熔点
(3)海水提溴过程中,先向浓缩海水中通入_____,将其中的Br﹣氧化,再用“空气吹出法”吹出Br2,并用纯碱吸收.已知纯碱吸收溴的主要反应是:Br2+Na2CO3+H2O→NaBr+NaBrO3+NaHCO3(未配平),则吸收1mol Br2,转移电子_____mol,反应中氧化产物为_____.
(4)已知:AlF3的熔点为1040℃,AlCl3在178℃升华.从物质结构的角度解释两者熔点相差较大的原因:__________
(5)HClO有很好的杀菌消毒效果.为增强氯水的杀菌能力,可以用饱和氯水与小苏打反应来达到目的,试用平衡移动原理解释其原因:_____________________。
【答案】3 ac Cl2或H2O2 1.67 NaBrO3 AlF3是离子晶体,AlCl3是分子晶体 ①氯水中存在Cl2+H2O![]() HCl+HClO,②盐酸是强酸,HClO和碳酸都是弱酸,且室温下Ki1(H2CO3)>Ki(HClO)>Ki2(H2CO3);③加入小苏打,盐酸能与之反应导致盐酸浓度下降,平衡向正向移动,而HClO不能与之反应,所以HClO浓度增大
HCl+HClO,②盐酸是强酸,HClO和碳酸都是弱酸,且室温下Ki1(H2CO3)>Ki(HClO)>Ki2(H2CO3);③加入小苏打,盐酸能与之反应导致盐酸浓度下降,平衡向正向移动,而HClO不能与之反应,所以HClO浓度增大
【解析】
(1)不同能级上的电子能量不同;
(2)元素的非金属性越强,其简单氢化物的稳定性越强,其最高价氧化物的水化物酸性越强,其单质的氧化性越强,据此分析解答;
(3)海水提溴时,一般用氯气或过氧化氢氧化Br﹣;根据溴元素化合价变化计算转移电子数;
(4) 离子晶体熔点高分子晶体;
(5)碳酸氢钠与盐酸反应,碳酸氢钠与次氯酸不反应;
(1)与氯元素同族的短周期元素为F元素,原子核外有7个电子,分别位于1s、2s、2p能级,有3种不同的能量;
(2)a.IBr中溴为﹣1价,说明Br得电子能力强, Br的非金属性较强,故选a;
b.HBr、HI的酸性不能作为判断的依据,故不选b;
c.HBr、HI的热稳定性越强,对应的非金属性越强,故选c;
d.Br2、I2的熔点属于物理性质,不能作为判断的依据,故不选d;
选a c;
(3)一般用氯气或过氧化氢氧化Br﹣,反应Br2+Na2CO3+H2O→NaBr+NaBrO3+NaHCO3中,Br元素化合价分别由0价变化为﹣1价、+5价,反应中Br2既是氧化剂又是还原剂,根据电子转移守恒可知,2×n氧化剂(Br2)=2×5×n还原剂(Br2),故n氧化剂(Br2):n还原剂(Br2)=5:1,故吸收1mol Br2时,转移的电子数为1mol×2×![]() ×5=mol=1.67mol,NaBrO3为氧化产物;
×5=mol=1.67mol,NaBrO3为氧化产物;
(4)AlF3的熔点为1040℃,AlCl3在178℃升华,原因是AlF3是离子晶体,AlCl3是分子晶体,离子晶体熔点高;
(5)氯水中存在Cl2+H2O![]() HCl+HClO,盐酸是强酸,HClO和碳酸都是弱酸,且室温下Ki1(H2CO3)>Ki(HClO)>Ki2(H2CO3),HCl和与碳酸氢钠反应,而HClO不反应,加入小苏打,盐酸能与之反应导致盐酸浓度下降,平衡向正向移动,而HClO不能与之反应,所以HClO浓度增大。
HCl+HClO,盐酸是强酸,HClO和碳酸都是弱酸,且室温下Ki1(H2CO3)>Ki(HClO)>Ki2(H2CO3),HCl和与碳酸氢钠反应,而HClO不反应,加入小苏打,盐酸能与之反应导致盐酸浓度下降,平衡向正向移动,而HClO不能与之反应,所以HClO浓度增大。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】从宏观现象探究微观本质是重要的化学学科素养。以亚硫酸纳(Na2SO3)为实验对象,探究其性质。实验如下:
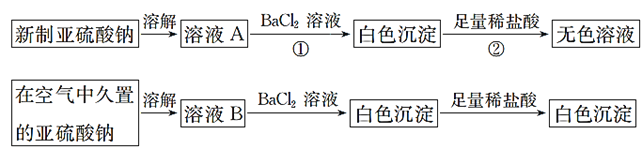
(1)写出上述实验中②的离子方程式:__________。
(2)通过上述实验可知,在空气中久置的亚硫酸纳固体中会混有____________ (填化学式)。
(3)亚硫酸纳晶体样品若变质,下列说法错误的是 _______________。
A.晶体表面变黄 B.其水溶液pH 将减小 C.其样品质量将增加
(4)将碳酸纳溶液加热到40 ℃通入二氧化硫饱和后,再加入等量的碳酸钠溶液,在避免与空气接触的情况下结晶可制得亚硫酸钠,该制备过程总反应的化学方程式 ___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】恒温,不同pH下,Fe(OH)3(s)与Cu(OH)2(s)分别在溶液中达到溶解平衡时,金属阳离子浓度随pH的变化如图所示。下列判断正确的是
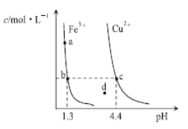
A.加适量盐酸可使溶液中c(Fe3+)由a点变到b点
B.c、d两点代表的溶液中,c(H+) c(OH-)不相等
C.a、b两点时,Fe(OH)3在溶液中均达到饱和
D.Ksp[Fe(OH)3] >Ksp[Cu(OH)2]
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】联碱法(侯氏制碱法)和氨碱法的生产流程简要表示如下:
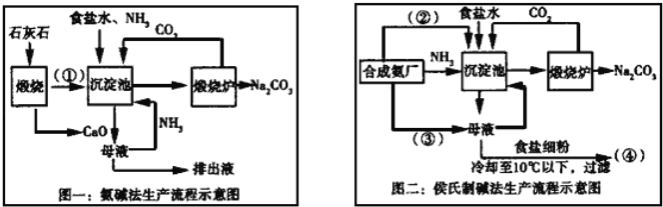
完成下列填空:
(1)写出化学式:②_____、③____
(2)从理论上分析,氨碱法生产过程中_____(选填“需要”、“不需要”)补充氨气,写出该工艺中生成CaCl2的化学方程式________________。
(3)对联碱法中从母液中提取氯化铵晶体的过程进行分析,所得结论合理的是______。
a.常温时氯化铵的溶解度比氯化钠小
b.通入氨气可把碳酸氢钠转化为碳酸钠,防止碳酸氢钠析出
c.加入食盐细粉目的是提高Na+的浓度,促进碳酸氢钠结晶析出
(4)取“侯氏制碱法”生产的纯碱样品5.500g,配成500mL溶液,取25mL溶液用0.1000mol/L的标准盐酸滴定(设其中的杂质不与盐酸反应),用酚酞作指示剂,三次滴定消耗盐酸的平均量为25.00mL.计算样品中纯碱的质量分数______。(已知25℃时0.1mol/L的NaHCO3溶液的pH约为8.3)某活动小组根据上述制碱原理,用如下所示装置(夹持装置省略)制备碳酸氢钠.
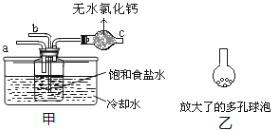
(5)实验时,须先从____管通入_____气体,再从_____管中通入_____气体。
(6)有同学建议在甲装置的b管下端连接乙装置,目的是________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苹果酸的结构简式为HOOC![]() CH2—COOH,下列说法正确的是
CH2—COOH,下列说法正确的是
A. 苹果酸中能发生酯化反应的官能团有2种
B. 1mol苹果酸可与3mol NaOH发生中和反应
C. 1mol苹果酸与足量金属Na反应生成生成1mol H2
D. HOOC—CH2—CH(OH)—COOH与苹果酸互为同分异构体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫化氢与浓硫酸发生如下反应:H2S+H2SO4(浓)→S↓+SO2↑+2H2O加热条件下,单质硫与浓硫酸又会发生如下反应:S+2H2SO4(浓)![]() 3SO2↑+2H2O
3SO2↑+2H2O
计算:
(1)若98%浓硫酸可表示为H2SO4aH2O,则a=__;若要把该浓硫酸转化为H2SO4H2O,则98%浓硫酸与加入水的质量比为_____。
(2)一定条件下,将0.1mol H2S气体通入足量浓硫酸中,生成b mol SO2,则 b的取值范围是_______。
(3)在50mL、4.0mol/L的NaOH溶液中,通入H2S气体并充分反应,然后,小心蒸发,得到不含结晶水的白色固体.通入H2S的物质的量为x mol,生成的白色固体的质量为7.9g,通过计算确定白色固体的可能成分及每种成分的质量(结果保留一位小数)_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物结构为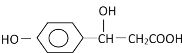 ,它可能发生的反应类型有( )
,它可能发生的反应类型有( )
①取代 ②加成 ③消去 ④水解 ⑤酯化 ⑥中和 ⑦氧化 ⑧加聚
A.①②③⑤⑥B.②③④⑤⑧C.③④⑤⑥⑦⑧D.①②③⑤⑥⑦
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水仙花所含的挥发油中含有丁香油酚、苯甲醇、苯甲醛、桂皮醇等成分。它们的结构简式如下:
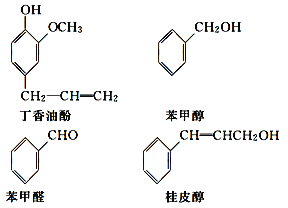
请回答下列问题:
(1)①丁香油酚中含氧的官能团是_____;丁香油酚可能具有的性质是_____(填字母)。
A.可与烧碱反应
B.只能与Br2发生加成反应
C.既可燃烧,也可使酸性KMnO4溶液褪色
D.可与NaHCO3溶液反应放出CO2气体
②从结构上看,上述四种有机物中与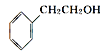 互为同系物的是____(填名称)。
互为同系物的是____(填名称)。
(2)苯甲醛经________(填反应类型)反应可得到苯甲醇。写出苯甲醛和银氨溶液反应化学方程式为___________________________________。
(3)由桂皮醇转化为丙的过程为(已略去无关产物)
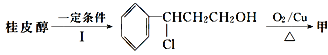
![]() 乙
乙![]() 丙
丙
如果反应Ⅱ为消去反应,则反应Ⅱ的条件是_______________,反应Ⅲ为加聚反应,则高聚物丙的结构简式为 _________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对二甲苯(PX)可发生如下反应生成对苯二甲酸(PTA)。下列有关说法错误的是
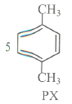 +12MnO4-+36H+
+12MnO4-+36H+![]()
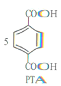 +12Mn2++28H2O
+12Mn2++28H2O
A.PTA是该反应的氧化产物B.消耗1molPX,共转移8mol电子
C.PX含苯环的同分异构体还有3种D.PTA与乙二醇可以发生缩聚反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com