


科目:高中化学 来源: 题型:
| A、3:8 | B、8:3 |
| C、3:1 | D、1:3 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
 现有前四周期六种元素X、Y、Z、E、F、G,它们的原子序数依次增大,除G外,其他五种元素都是短周期元素.X、Y、E三种元素组成的化合物是实验室常用燃料,也是一种家庭常见饮品的主要成分.取F的化合物做焰色反应实验,其焰色呈黄色,G的单质是生活中常见的一种金属,GE是黑色固体.G2E是红色固体.请回答下列问题:
现有前四周期六种元素X、Y、Z、E、F、G,它们的原子序数依次增大,除G外,其他五种元素都是短周期元素.X、Y、E三种元素组成的化合物是实验室常用燃料,也是一种家庭常见饮品的主要成分.取F的化合物做焰色反应实验,其焰色呈黄色,G的单质是生活中常见的一种金属,GE是黑色固体.G2E是红色固体.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
 A、B、C、D、E为周期表中前四周期的元素,其核电荷数依次增大,A、B、C为同一周期元素,AC与B2互为等电子体,D原子中s电子总数与p电子总数相等,且与B能形成离子化合物D3B2,五种元素的核电荷数之和为62.请回答下列问题:
A、B、C、D、E为周期表中前四周期的元素,其核电荷数依次增大,A、B、C为同一周期元素,AC与B2互为等电子体,D原子中s电子总数与p电子总数相等,且与B能形成离子化合物D3B2,五种元素的核电荷数之和为62.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 2 |
| A、H2的燃烧热为241.8kJ/mol | ||
B、H2(g)+
| ||
| C、2H2(g)+O2(g)=2H2O(g);△H>-241.8kJ/mol | ||
D、1molH2与
|
查看答案和解析>>
科目:高中化学 来源: 题型:
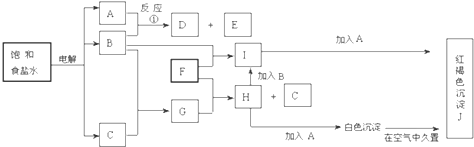
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com