
下列有关物质用途的说法中,正确的是( )
A.玻璃容器可长期盛放各种酸 B.硝酸常用作金属铜加工前的酸洗
C.碳酸钠可用于治疗胃酸过多 D.三氧化二铁常用于生产红色油漆和涂料
科目:高中化学 来源: 题型:
某化学学习小组设计如图实验装置(夹持装置略去)制备Cl2,并探究氯气的相关性质.

(1)若A装置中固体药品为MnO2,其化学方程式为
若A装置中固体药品为KClO3,则反应中每生成1molCl2时转移电子的物质的量为 mol.
(2)装置B的作用:
(3)装置C的作用是验证氯气是否具有漂白性,l处是湿润的有色布条,则Ⅱ、Ⅲ处应加入的物质分别是 .
(4)设计装置D、E的目的是比较氯、溴、碘的非金属性。但有同学认为该设计不够严密,他的理由可能 。
(5)请用化学方程式说明装置F的作用 。
(6)甲同学提出,装置F中的试剂可改用过量的Na2SO3溶液,乙同学认真思考后认为此法不可行.请用离子方程式解释乙认为不可行的原因:
查看答案和解析>>
科目:高中化学 来源: 题型:
在隔绝空气的条件下,某同学将一块部分被氧化的钠块用一张已除去氧化膜、并用针刺一些小孔的铝箔包好,然后放入盛满水且倒置于水槽中的容器内。待钠块反应完全后,在容器中仅收集到1.12 L氢气(标准状况),此时测得铝箔质量比反应前减少了0.27 g,水槽和容器内溶液的总体积为2.0 L,溶液中NaOH的浓度为0.050 mol·L-1(忽略溶液中离子的水解和溶解的氢气的量)。
(1)写出该实验中发生反应的化学方程式:
;
(2)试通过计算确定该钠块中钠元素的质量分数为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列物质的保存方法正确的是
①少量金属钠保存在冷水中②浓硝酸盛放在无色试剂瓶中
③少量金属钾保存在煤油中④氢氧化钠溶液盛放在带有橡胶塞的试剂瓶中
⑤氯水存放在带玻璃塞的无色细口瓶中⑥碳酸钠固体保存在带橡胶塞的细口瓶中
A.②③④ B.③④⑥ C.③④ D.①③④
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法不正确的是( )。
A.用加热法可除去Na2CO3中的NaHCO3
B.Na2CO3的热稳定性大于NaHCO3
C.可用石灰水区分Na2CO3与NaHCO3溶液
D.小苏打可中和胃酸、热纯碱可除去油污
查看答案和解析>>
科目:高中化学 来源: 题型:
很多微粒具有六元环的结构。
Ⅰ.六氯环三磷腈分子中包含一个六元环,是橡胶生产中的重要中间体,其结构如图所示,其熔点为113℃,在减压下,50℃即可升华。在有机溶剂中,六氯环三磷腈可由五氯化磷与氯化铵反应制得,反应的方程式为3PCl5+3NH4Cl====P3N3Cl6+12HCl。

(1)比较磷元素和氯元素的第一电离能:P______Cl(填“>”或“<”)。
(2)在上述反应中断裂的化学键有________(填序号)。
A.离子键 B.配位键 C.极性键 D.非极性键
(3)P3N3Cl6的晶体类型为___________。
Ⅱ.1,3-戊二酮通过两步变化,也可以形成六元环,增加了分子的稳定性,其变化如图所示:
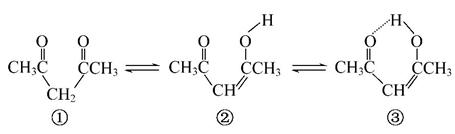
(4)由①转化为②时,π键数目________(填“增加”“减小”或“不变”)。
(5)由②转化为③时,③比②多增加了一种微粒间作用力,该作用力是__________。
Ⅲ.S和Ge可构成[Ge4S10]4-,锗和硫原子也连结成六边形结构,如图所示。

(6)锗原子的价电子排布式为_______。
(7)图中涂黑的微粒代表__________元素。
查看答案和解析>>
科目:高中化学 来源: 题型:
MOH和ROH两种一元碱的溶液分别加水稀释10n倍时,pH变化与n的关系如图所示。下列叙述中正确的是
( )

A.MOH和ROH都是强碱
B.稀释前,[ROH]=10[MOH]
C.常温下pH之和为14的醋酸和ROH溶液等体积混合,所得溶液呈碱性
D.在x点,[M+]=[R+]
查看答案和解析>>
科目:高中化学 来源: 题型:
科学家最近在-100 ℃的低温下合成一种烃X,此分子的结构如图所示(图中的连线表示化学键)。下列说法正确的是 ( )
A.充分燃烧等质量的X和甲烷,X消耗氧气较多
B.X是一种常温下能稳定存在的液态烃
C.X和乙烷类似,都容易发生取代反应
D.X既能使溴的四氯化碳溶液褪色又能使酸性KMnO4溶液褪色

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com