
����Ŀ���о�̼�������仯�����ת�����ڻ����ĸ������ش����塣
��1��������ԭ������NOx��ת�����£�![]()
��֪��NO(g)+O3(g)=NO2(g)+O2(g) ��H=-200.9kJ/mol
2NO(g)��O2(g)=2NO(g) ��H=-116.2kJ/mol
��ӦI���Ȼ�ѧ����ʽΪ________________��
��2���������뽫CO�����з�Ӧ��ȥ��2CO(g)=2C(s)+O2(g) ��H>0����������������ܷ�ʵ�֣�______����ǡ���) ��������_____________��
��3��һ�������£�CO�����ĩ״�����������������ɼ����ơ���֪����ʱ������ĵ���ƽ�ⳣ��Ka=1.70��10-4��
�� �����Ƶ�ˮ��Һ�ʼ��ԣ��������ӷ�Ӧ����ʽ��ʾ��ԭ��___________��
�� ��20mL 0.1mol/L�ļ�������Һ�еμ�10ml 0.1mol/L�����ᣬ���Һ��______�ԣ���ᡱ�������Һ������Ũ�ȴӴ�С��˳��Ϊ______________��
��4������̿Ҳ�����ڴ�������β���е�NO����2L�����ܱ������м���0.1000molNO��2.030mol�������̿������A��B�������壬�ڲ�ͬ�¶��²��ƽ����ϵ�и����ʵ����ʵ������±���

�ٸ÷�Ӧ������ӦΪ________(����ȡ����ȡ�)��Ӧ��
�� 200��ʱ��ƽ���������������ٳ���0.1molNO���ٴ�ƽ���NO�İٷֺ�����_____�������������С�����䡱����
�ۼ��㷴Ӧ��ϵ��335�� ʱ��ƽ�ⳣ��_______��
���𰸡���1�� 3NO(g)+O3(g)===3NO2(g) ��H=��317.1 kJ��mol-1
��2���� �÷�Ӧ���������ؼ��ķ�Ӧ,����G=��H -T����S,G>0
��3����HCOO����H2O![]() HCOOH + OH��
HCOOH + OH��
���� c (Na+)>c(HCOO��)>c (Cl��)>c(H+)>c(OH-)
��4���ٷ��� �ڲ��� �� 0.25
��������(1)��Ӧ��NO(g)��O3(g)���ݸ�˹���ɣ���NO(g)+O3(g)�TNO2(g)+O2(g)��H=-200.9kJ/mol����2NO(g)+O2(g)�T2NO(g)��H=-116.2kJ/mol����Ŀ�귴Ӧ�ķ�Ӧ�ȵ��ڢ�+�ڣ�����I���Ȼ�ѧ����ʽΪ3NO(g)+O3(g)�T3NO2(g)��H=-317.1 kJmol-1��
(2)���ݡ�G=��H-T��S�жϷ�Ӧ�ܷ��Է����У������G��0����Ӧ���Է����У���G��0����Ӧ�����Է����У�2CO(g)=2C(s)+O2(g)���÷�Ӧ���������ؼ��ķ�Ӧ������G=��H-T��S��G��0������ʵ�֣�
(3)�ټ�������ǿ�������Σ�ˮ��ʼ��ԣ�����ˮ��Һ�ʼ��ԣ����ӷ�Ӧ����ʽ��ʾ��ԭ��HCOO-+H2O![]() HCOOH+OH-��
HCOOH+OH-��
����20mL 0.1mol/L�ļ�������Һ�еμ�10ml 0.1mol/L�����ᣬ�õ������ʵ���Ũ�ȵļ��ᡢ�����ƺ��Ȼ��ƵĻ��Һ���Լ���ĵ���Ϊ������Һ�����ԣ���Һ������Ũ�ȴӴ�С��˳��Ϊc(Na+)��c(HCOO-)��c(Cl-)��c(H+)��c(OH-)��
(4)���¶�����ƽ�������ƶ�����������Ӧ�Ƿ��ȷ�Ӧ��
����200��ʱ�������ʵ�����ϵ��֪����Ӧ����ʽΪ��2NOA+B����������ļ�������ȣ���ƽ���������������ٳ���0.1molNO���൱������ѹǿ��ƽ�ⲻ�ƶ�������NO�İٷֺ��������䣻
��ƽ�ⳣ������ƽ��ʱ�������Ũ����֮�����Ϸ�Ӧ��Ũ����֮��������K= =0.25��
=0.25��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ˮ��Һ�еĸ���������Ϊ����������ԭ��Ӧ�����ܴ���������ǣ� ��
A.Na+��Ba2+��Cl��SO42- B. Ca2+��HCO3��C1��K+
C.MnO4��K+��I��H+ D. H+ ��Cl ��Na+ ��CO32
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Fe��Cu��Fe2+��Fe3+��Cu2+ʢ��ͬһ�����г�ַ�Ӧ����Ӧ��Fe��ʣ�࣬���������������ڵĵ��ʻ�����ֻ���ǣ� ��
A.Cu��Fe3+
B.Fe2+��Fe3+
C.Cu��Cu2+
D.Cu��Fe2+
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���о�CO2�����öԴٽ���̼���Ĺ���������Ҫ���塣
��1����CO2�뽹̿��������CO��CO�����������ȡ�
����֪��Fe2O3(s)��3C(ʯī)=2Fe(s)��3CO(g) ��H1��akJ��mol��1
C(ʯī)��CO2(g)=2CO(g) ��H2��bkJ��mol��1
��CO��ԭFe2O3(s)���Ȼ�ѧ����ʽΪ______________��
��2����CO2ת��Ϊ�״����Ȼ�ѧ����ʽΪ�� CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) ��H
CH3OH(g)+H2O(g) ��H
ȡһ�����CO2��H2�Ļ������(���ʵ���֮��Ϊ1��3)����������ܱ������У�����������Ӧ��
�����������˵����Ӧ�Ѵ�ƽ��״̬����________������ĸ����
A.�����������ܶȲ��� B.������������ѹǿ���ֲ���
C.���Ⱥ���ʱ��ƽ�ⳣ������ D.v��(CH3OH)=3v��(H2)
�ڷ�Ӧ�����в�ü״������������(CH3OH)�뷴Ӧ�¶�T�Ĺ�ϵ��ͼ��ʾ����÷�Ӧ�Ħ�H______0(�>������<������)��
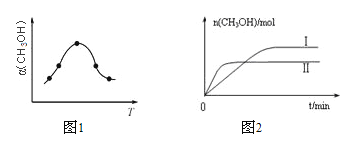
�������ֲ�ͬ�����·�����Ӧ�����CH3OH�����ʵ�����ʱ��仯��ͼ��ʾ������I�����Ӧ��ƽ�ⳣ����С��ϵΪK��_____K��(�>������<������)��
��3����CO2Ϊԭ�ϻ����Ժϳɶ������ʡ�
����ͼ��ģ�⡰�����Ƽ����ȡNaHCO3�IJ���װ�á�����������_____��ͨ��NH3���壬Ȼ������_______��ͨ��CO2���塣
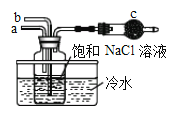
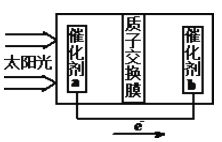
���˹���������ܹ�����̫������CO2��ˮ�Ʊ���ѧԭ�ϣ���ͼ��ͨ���˹���������Ʊ�HCOOH��ԭ��ʾ��ͼ����д������b���ĵ缫��Ӧʽ��________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���й���Ԫ�ص�����˵������ȷ����
A. �������Խ��Խ�����ڽ���
B. ��Ԫ���ֳ�Ϊ������Ԫ��
C. Ӥ�������ȱ��������״����
D. ��������0.01%����Ԫ�أ�����ά����������ٽ������ͷ���������Ҫ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����̼�������ס����Ԫ����ɵĵ����ʣ������ھ������������պ�����������ᣬ��Ӧ�����ȷ���ǣ� ��
A. ̼��̼�� B. �������� C. �������� D. ��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ����������������Ҫ��������
������һ��������Ũ������Ũ����Ļ����,���뷴Ӧ���У�
���������µĻ��������μ���һ�����ı�,�����,��Ͼ��ȣ�
����50~60���·�����Ӧ,ֱ����Ӧ������
�ܳ�ȥ������,�ֲ�Ʒ����������ˮ��5%��NaOH��Һϴ��,�����������ˮϴ�ӣ�
�ݽ�����ˮCaCl2�����Ĵ���������������,�õ�����������
��ش���������:
��1������һ������Ũ������Ũ��������ʱ,����ע��������___________��
��2���������,Ϊ��ʹ��Ӧ��50~60���½���,���õķ�����____________��
��3���������ϴ�Ӵ�������ʹ�õ�������_____________��
��4��������дֲ�Ʒ��5%��NaOH��Һϴ�ӵ�Ŀ����__________________��
��5��д�����������ķ���ʽ________��������������ɫ���ܶȱ�ˮ_____(�С����),����________��ζ����״Һ�塣
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������Ȼ����У������ɵ���ֱ�ӻ����Ƶã��ֿ��ɽ��������ᷴӦ�Ƶõ��ǣ�������
A.CuCl2
B.FeCl2
C.FeCl3
D.AlCl3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��I������������ֵ����Ϊ25��ʱ��
��1��ijŨ�ȵ�NH3��H2O��Һ�У���ˮ�����c(H+)=1��10-12mol/L,����Һ�� pH=_________
��2����pH=3��H2SO4 ��Һ��pH=12��NaOH��Һ���, ��Ϻ�������Һ��PH=10����H2SO4 ��Һ��NaOH��Һ�������Ϊ______________
��3����0.02mol/L��MgCl2��Һ�м���NaOH���壬��Ҫ����Mg(OH)2��������Һ��pH���Ϊ__________����֪Ksp[Mg(OH)2]=3.2��10-11,lg2.5=0.4��
II����1���μ���϶��![]() ��ʹ�������ʼ��ԣ�����������������ͨ��ʩ������ʯ���ĩ����Ҫ����CaSO4������ˮ�������������ļ��ԡ�д���ù����з�����Ӧ�Ļ�ѧ����ʽ_______________________________
��ʹ�������ʼ��ԣ�����������������ͨ��ʩ������ʯ���ĩ����Ҫ����CaSO4������ˮ�������������ļ��ԡ�д���ù����з�����Ӧ�Ļ�ѧ����ʽ_______________________________
��2��![]() ��һ����ɫ��ɫҺ�壬��ˮ���ҷ�Ӧ�õ�����������Ȼ��⣬��һ�ֳ��õ���ˮ������
��һ����ɫ��ɫҺ�壬��ˮ���ҷ�Ӧ�õ�����������Ȼ��⣬��һ�ֳ��õ���ˮ������![]() ��
��![]() ��ϲ����ȣ��ɵõ���ˮ
��ϲ����ȣ��ɵõ���ˮ![]() ���õ���ˮ
���õ���ˮ![]() �Ļ�ѧ����ʽΪ______________________________
�Ļ�ѧ����ʽΪ______________________________
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com