
化学反应N2+3H2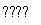 2NH3的能量变化如图所示,该反应的热化学方程式是 )。
2NH3的能量变化如图所示,该反应的热化学方程式是 )。
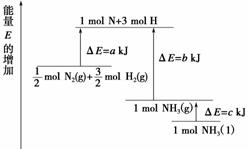
A.N2g)+3H2g)2NH3l) ΔH=2a-b-c)kJ·mol-1
B.N2g)+3H2g)2NH3g) ΔH=2b-a)kJ·mol-1
C.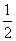 N2g)+
N2g)+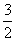 H2g)NH3l) ΔH=b+c-a)kJ·mol-1
H2g)NH3l) ΔH=b+c-a)kJ·mol-1
D.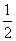 N2g)+
N2g)+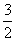 H2g)NH3g) ΔH=a+b)kJ·mol-1
H2g)NH3g) ΔH=a+b)kJ·mol-1
 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案科目:高中化学 来源: 题型:
NA表示阿伏加德罗常数的值,下列说法中正确的是(双选)( )
A.100 mL 1 mol·L-1 Na2CO3溶液中溶质离子的总数小于0.3NA
B.若120 g的墨粉(只含碳)能打a个字,则平均每个字约含有10NA/a个碳原子
C.25℃、101 kPa时,0.1NA个H2分子完全燃烧生成液态水,放出a kJ热量,表示氢气燃烧热的热化学方程式为H2(g)+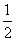 O2(g)===H2O(l) ΔH=+10a kJ·mol-1
O2(g)===H2O(l) ΔH=+10a kJ·mol-1
D.常温下28 g 14CO中含有14NA个电子
查看答案和解析>>
科目:高中化学 来源: 题型:
已知反应mX(g)+nY(g)  qZ(g) ΔH>0,m+n>q,在恒容密闭容器中反应达到平衡时,下列说法正确的是( )
qZ(g) ΔH>0,m+n>q,在恒容密闭容器中反应达到平衡时,下列说法正确的是( )
A.升高温度,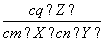 增大
增大
B.降低温度,混合气体的平均相对分子质量增大
C.通入稀有气体,压强增大,平衡向正反应方向移动
D.X的正反应速率是Y的逆反应速率的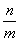 倍
倍
查看答案和解析>>
科目:高中化学 来源: 题型:
某温度时,在一个容积为2 L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示。根据图中数据,试填写下列空白:
(1)该反应的化学方程式为____________________________________。
(2)反应开始至2 min,气体Z的反应速率为_____________________。
(3)若X、Y、Z均为气体,反应达到平衡时:
①压强是开始时的________倍;
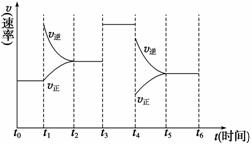 ②若此时将容器的体积缩小为原来的
②若此时将容器的体积缩小为原来的 倍,达到平衡时,容器内温度将升高(容器不与外界进行热交换),则该反应的正反应为________反应(填“放热”或“吸热”)。
倍,达到平衡时,容器内温度将升高(容器不与外界进行热交换),则该反应的正反应为________反应(填“放热”或“吸热”)。
(4)若上述反应在2 min后的t1~t6内反应速率与反应时间图像如右,在每一时刻均改变一个影响反应速率的因素,则( )
A.在t1时增大了压强 B.在t3时加入了催化剂
C.在t4时降低了温度 D.t2~t3时X的转化率最高
查看答案和解析>>
科目:高中化学 来源: 题型:
为探究NaHCO3、Na2CO3与1 mol·L-1盐酸反应设两反应分别是反应Ⅰ、反应Ⅱ)过程中的热效应,进行实验并测得如下数据:
| 序号 | 液体 | 固体 | 混合前温度 | 混合后最高温度 |
| ① | 35 mL水 | 2.5 g NaHCO3 | 20 ℃ | 18.5 ℃ |
| ② | 35 mL水 | 3.2 g Na2CO3 | 20 ℃ | 24.3 ℃ |
| ③ | 35 mL盐酸 | 2.5 g NaHCO3 | 20 ℃ | 16.2 ℃ |
| ④ | 35 mL盐酸 | 3.2 g Na2CO3 | 20 ℃ | 25.1 ℃ |
下列有关说法正确的是 )。
A.仅通过实验③即可判断反应Ⅰ是吸热反应
B.仅通过实验④即可判断反应Ⅱ是放热反应
C.通过实验可判断出反应Ⅰ、Ⅱ分别是吸热反应、放热反应
D.通过实验可判断出反应Ⅰ、Ⅱ分别是放热反应、吸热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
在绝热、恒容的密闭容器中进行反应2NOg)+2COg)2CO2g)+N2g),下列示意图正确且能高效能反应在进行到t1时刻平衡状态的是双选) )。
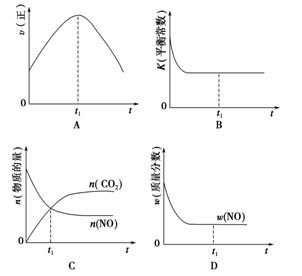
查看答案和解析>>
科目:高中化学 来源: 题型:
某研究性学习小组在网上收集到信息:钠、镁等活泼金属都能在CO2气体中燃烧。
他们对钠在CO2气体中燃烧后得到的白色产物进行了如下探究:
【实验操作】 将燃烧的钠迅速伸入装满CO2的集气瓶中,钠在其中继续燃烧,反应后冷却,瓶底有黑色颗粒,瓶壁上附着白色物质。
【提出假设】
假设1:白色物质是Na2O。
假设2:白色物质是Na2CO3。
假设3:白色物质是Na2O和Na2CO3的混合物。
【设计方案】 该小组对燃烧后生成的白色物质进行如下探究:
| 实验方案 | 实验操作 | 实验现象 | 结论 |
| 方案1 | 取少量白色物质于试管中,加入适量水,振荡,样品全部溶于水,向其中加入无色酚酞试液 | 溶液变成红色 | 白色物质为Na2O |
| 方案2 | ①取少量白色物质于试管中,加入适量水,振荡,样品全部溶于水,向其中加入过量的CaCl2溶液。 ②静置片刻,取上层清液于试管中,滴加无色酚酞试液 | ①出现白色沉淀。 ②无明显现象 | 白色物质为Na2CO3 |
请回答下列问题:
(1)写出金属镁与二氧化碳反应的化学方程式:____________________________________________________
____________________________________________________。
(2)甲同学认为方案1得到的结论不正确,其理由是____________________________________________________
____________________________________________________。
(3)乙同学认为方案2得到的结论正确,白色物质为____________________________________________________。
(4)钠在二氧化碳中燃烧的化学反应方程式为____________________________________________________
____________________________________________________。
(5)丙同学认为白色物质有可能是氢氧化钠。你是否同意丙同学的观点,并简述理由:____________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知: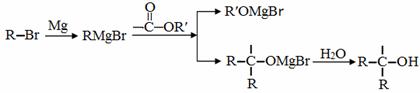
A是一种重要的化工原料,能使溴水反应褪色,且分子内所有的原子都在一条直线上,在不同的条件下,A可以转化为烃B和烃C,B和C的核磁共振氢谱中都只有一个吸收峰,B能使溴水反应褪色而C不能使溴水反应褪色。A~J分别代表一种有机物,并有如下的转化关系:
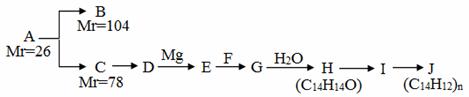
回答下列问题:
(1)A的结构简式为________________;
(2)B的结构简式为_________________;
(3)反应C→D所需要的试剂是_________________________;
(4)H不能发生催化氧化,H的结构简式是____________________________________;
(5) I中的官能团名称是___________________;
(6) I中可能含有的杂质是_____________________(写结构简式);
(7)写出I→J的反应方程式________________________________________________;
(8)H有多种同分异构体,符合下列条件的同分异构体有________种。
①能与FeCl3溶液显紫色;②有二联苯结构;③二联苯上有两个侧链。
其中核磁共振氢谱中吸收峰最少的结构简式是____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
对σ键的认识不正确的是( )
A.σ键不属于共价键,是另一种化学键
B.S-Sσ键与S-Pσ键的对称性相同
C.分子中含有共价键,则至少含有一个σ键
D.含有π键的化合物与只含σ键的化合物的化学性质不同
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com